Résumé
L’échographie est une technique performante, sans danger, peu coûteuse et facilement accessible qui a pris une place majeure dans l’imagerie de l’appareil moteur en une vingtaine d’années. Grâce à de multiples innovations : sondes multifréquences de haute définition, sommation en temps réel d’images issues de plusieurs faisceaux d’ultrasons, utilisation des fréquences harmoniques, Doppler puissance, champs de vue élargis…, les images, grossières à l’origine, sont devenues détaillées et riches d’informations. Parallèlement, les connaissances écho-anatomiques se sont considérablement élargies et affinées et, grâce à l’acquis de l’imagerie par résonance magnétique et de la tomodensitométrie, la sémiologie échographique a beaucoup gagné en rigueur et précision. Les auteurs font le point de l’échographie diagnostique et interventionnelle dans la pathologie de l’appareil moteur.
Summary
Sonography is a safe, inexpensive and readily accessible technique which has acquired a major place in musculoskeletal imaging over the past two decades. Thanks to recent technical innovations such as high-definition multifrequency probes, compound effect, use of harmonic frequencies, power Doppler, and extended field of view, today’s sonographic images are extremely precise. At the same time, based on magnetic resonance imaging (MRI) and computed tomography (CT) acquisitions, the sonographic anatomy has become broader and more detailed, and the sonographic semiology is more precise and reliable. In this article the authors evaluate current uses of diagnostic and interventional sonography in musculoskeletal disorders.
INTRODUCTION
Une simple comparaison entre les premières échographies de l’appareil moteur et les examens actuels (figure 1) permet de réaliser les progrès effectués en quelques années ainsi que la clairvoyance des pionniers de cette technique qui avaient compris son immense potentiel et prévu la place prépondérante qu’elle occupe aujourd’hui dans l’imagerie musculo-squelettique.
1 a 1 b FIG. 1ab. — a : tendon calcanéen normal (1988). La silhouette du tendon (têtes de flèches) est analysable, mais sa structure interne reste mal définie. b : tendinose corporéale du tendon tibial antérieur (2004). Sa structure interne, normale par endroit (étoile noire) est désorganisée en d’autres (étoile creuse).
HISTORIQUE
L’échographie médicale date des années 1960, les premières bases de la sémiologie de l’appareil moteur [1, 2] des années 70, et les premières descriptions des pathologies de cet appareil des années 75 [3]. À la fin des années 80, l’essentiel de la sémiologie des grandes lésions musculo-squelettiques était décrite [4, 5, 6]. Les débuts, difficiles, de l’échographie de l’appareil moteur furent néanmoins entachés par de multiples erreurs diagnostiques, ce qui entraîna une désillusion chez les premiers prescripteurs et un certain rejet de la méthode. Le développement en parallèle de la tomodensitométrie et de l’imagerie par résonance magnétique accentua cette désaffection. Depuis une dizaine d’années, l’échographie des parties molles est en pleine expansion grâce à un matériel performant, des connaissances anatomiques considérablement affinées et une sémiologie qu’ont précisée de nombreux travaux de corrélation entre échographie, anatomie et autres techniques d’imagerie.
La France et l’Europe de l’Ouest ont été particulièrement actives dans cette progression, notamment par le biais de sociétés d’imagerie spécialisées jeunes et dynamiques, telles le GEL (Groupe des Échographistes Locomoteurs). À l’heure actuelle l’échographie est devenue, couplée aux clichés simples, l’examen de première intention dans un grand nombre d’affections quotidiennes de l’appareil moteur.
BASES TECHNOLOGIQUES
Les variations de pression de l’air qui vibre à des fréquences comprise entre 20 et 20.000 périodes par secondes (Hertz) sont perçues par l’oreille humaine sous forme de sons. Au-delà, ce sont des ultrasons (US). Les US utilisés en échographie ont une fréquence comprise entre deux ou trois MHz et une vingtaine de MHz. Ils sont alternativement émis et reçus par des cristaux piézo-électriques, regroupés pour former une sonde, qui permettent d’obtenir l’image d’un plan de coupe ou, plus exactement, d’une tranche puisque l’image a une certaine épaisseur. La puissance des calculateurs et la technologie des sondes fournissent actuellement des images de haute définition en temps réel, autorisant l’étude détaillée de structures en mouvement. Ce caractère dynamique de l’échographie, original, particulièrement utile dans l’étude de l’appareil moteur, n’existe ni en tomodensitométrie, ni en imagerie par résonance magnétique. La vitesse de propagation des US dans l’eau et les tissus mous, rapport de leur longueur d’onde par leur fréquence, est pratiquement constante. Les US de courte longueur d’onde, qui fournissent les images les plus détaillées, ont donc une fréquence élevée. Or, plus la fréquence des US est élevée, moins ils sont pénétrants. L’opérateur doit donc choisir en permanence entre des US de haute fréquence, donnant des images précises mais sur une faible profondeur, ou des US de fréquence plus basse, à l’origine d’images moins fines, sur une étendue plus vaste. Comme les sons, les US qui se réfléchissent sur l’interface entre deux milieux d’impédances acoustiques différentes, créent un écho de retour. Un milieu
qui génère de nombreux échos est dit hyperéchogène, hypoéchogène s’il génère peu d’échos, et anéchogène s’il ne génère pas d’échos du tout. L’eau est anéchogène, ainsi que les liquides biologiques fluides. Les liquides épais sont d’échogénicité variable. La graisse est hyperéchogène. Le muscle est d’échogénicité moyenne. Si la différence d’impédance entre deux structures est très importante, la quasi-totalité des US se réfléchit sur l’interface entre ces deux milieux et le plus éloigné de la sonde n’est plus analysable. C’est le cas pour l’air où la vitesse de propagation des US est faible, ou pour l’os où elle est élevée. Ces milieux constituent une barrière infranchissable pour les US utilisés en échographie. Il faut donc utiliser un gel de couplage pour supprimer toute interposition d’air entre la sonde et la peau et limiter l’étude échographique aux parties molles situées entre la peau et le squelette dont seule la corticale superficielle peut être analysée.
Deux types d’effet Doppler sont utilisés en échographie de l’appareil moteur. Le Doppler couleur qui précise le sens du déplacement et la vitesse du sang circulant, mais nécessite des flux assez rapides et est dépendant de l’orientation de la sonde par rapport au vaisseau, et le Doppler puissance, basé sur l’énergie du signal rétrodiffusé par les hématies dont le nombre et la vitesse du sang déterminent l’intensité du signal. Ce type de Doppler, qui a le meilleur rapport signal/bruit, est peu dépendant de l’orientation du vaisseau et étudie les flux lents, est le plus adapté à l’étude des parties molles superficielles (figure 7).
EFFETS INDÉSIRABLES
Lorsqu’ils traversent les tissus, les US provoquent une élévation de température et une variation de la pression locale. Cette dernière, susceptible d’entraîner une destruction tissulaire en cas d’implosion de bulles aériques (dans les poumons ou l’intestin), concerne peu l’échographie des membres. Elle pourrait être prise en compte pour l’étude de la paroi thoracique ou abdominale ou pour les examens de l’appareil moteur chez la femme enceinte. Bien qu’à l’heure actuelle, il n’ait pas été rapporté d’effet biologique confirmé lors des échographies humaines, de telles conséquences ont été décrites chez des modèles animaux lors d’expositions proches de celles utilisées chez l’homme. Des normes de sécurité ont donc été établies [7] concernant essentiellement l’échographie fœtale.
DERNIÈRES INNOVATIONS TECHNIQUES
Les sondes dédiées à l’étude des parties molles superficielles atteignent aujourd’hui un haut niveau technologique : les deux principaux progrès récents concernent la direction et la fréquence des US, ainsi que leur champ d’étude. Par ailleurs, des produits de contraste ultrasonographiques sont récemment apparus sur le marché.
Habituellement, les US sont émis perpendiculairement à la surface des sondes linéaires. Ils abordent à angle droit les structures parallèles à la peau et entraînent
peu d’artéfacts d’anisotropie (hypoéchogénicité artéfactuelle constatée lorsque les ultrasons abordent obliquement certaines structures anatomiques normalement hyperéchogènes). Ces mêmes sondes, à la demande, produisent des US divergents qui couvrent un champ plus large, ou des US obliques, qui permettent d’aborder perpendiculairement certaines structures inclinées. Des sondes peuvent émettre successivement des faisceaux d’ultrasons dans plusieurs directions différentes et sommer en temps réel les images ainsi obtenues, de façon à en augmenter le rapport signal/bruit et à minimiser les artéfacts d’anisotropie (effet « compound »).
La fréquence d’émission de la majorité des sondes actuelles peut être réglée entre 7 et 15 MHz environ (« sondes multi-fréquences »), ce qui évite d’avoir à choisir entre une sonde de fréquence élevée mais pénétration faible, et une sonde de fréquence basse plus pénétrante. L’utilisation des fréquences harmoniques (échos dont la fréquence est un sous-multiple de la fréquence d’émission), qui augmente considérablement le rapport signal /bruit, surtout en profondeur, est actuellement largement répandue.
Le champ de vue étudié par les sondes échographiques superficielles est étroit, ce qui fournit une imagerie segmentaire déroutante. Pour agrandir ce champ, des sondes plus larges (jusqu’à 9 cm) sont disponibles, au prix d’une moins bonne définition. Il est également possible en déplaçant la sonde de sommer en temps réel les images obtenues, de façon à obtenir une vue panoramique d’une vaste zone anatomique, un peu comme on réunit plusieurs photographies pour obtenir un paysage entier. Cette technique de balayage (figure 2) est particulièrement utile en pathologie traumatique et tumorale, de façon à repérer et mesurer précisément des lésions étendues.
De nouveaux types de sondes visualisent en trois dimensions la zone anatomique étudiée. Ces sondes commencent à être utilisées en pathologie digestive et obstétricale, mais pas, à notre connaissance, pour l’exploration de l’appareil moteur, moins adapté aux sondes 3D du fait de sa morphologie moins compacte et de la présence du squelette.
Les produits de contraste échographiques, à base de microbulles encapsulées, augmentent la réflectivité du sang ou sont captés par un organe particulier. Ces produits, encore du domaine de la recherche en pathologie viscérale ou cardiovasculaire, sont très peu exploités à ce jour en pathologie de l’appareil moteur.
PARTICULARITÉS DE L’ÉCHOGRAPHIE DE L’APPAREIL MOTEUR
L’échographie de l’appareil moteur fournit des images anatomiques fragmentaires.
Cet aspect morcelé des images constitue un obstacle indéniable aussi bien pour le diagnostic que pour la transmission de l’information. D’où l’importance d’une connaissance anatomique approfondie, du repérage minutieux des images, de leur annotation détaillée et d’utilisation de plans de coupes simples et connus. Un important effort actuel s’oriente dans le sens d’une standardisation des examens échographiques de l’appareil moteur.
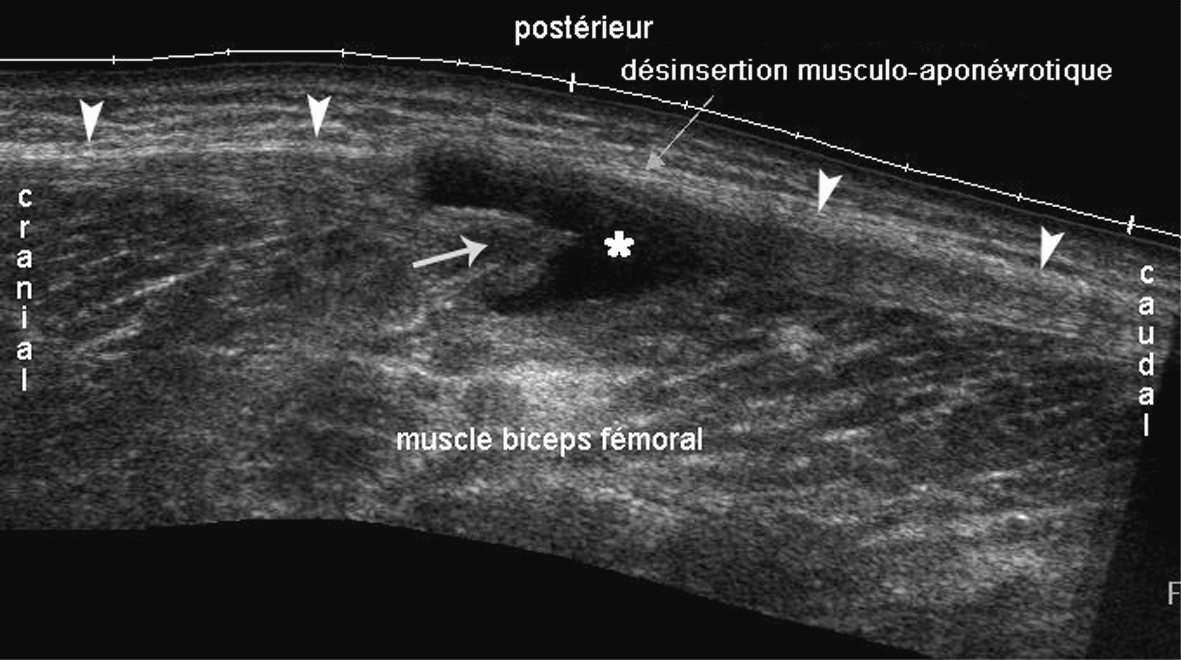
FIG. 2. — Désinsertion musculo-aponévrotique du biceps fémoral. Coupe longitudinale en balayage.
Les fibres musculaires désinsérées de l’aponévrose (têtes de flèches) se sont rétractées (flèche) et il existe un hématome hypoéchogène (astérisque) dans la zone de désinsertion.
La critique la plus souvent formulée à l’encontre de l’échographie est son caractère dépendant de l’opérateur. En fait, de l’intervention chirurgicale à la simple consultation, tous les actes médicaux sont opérateur-dépendants. Cette dimension humaine, reflet de leur difficulté, leur donne à la fois leur noblesse et leur fragilité.
APPLICATIONS PATHOLOGIQUES
L’échographie est actuellement l’imagerie de base des muscles, des tendons, de nombreux ligaments, des nerfs superficiels, des masses et des corps étrangers superficiels. Elle est un appoint précieux dans l’étude des articulations et de la surface des os. En visualisant en temps réel le trajet des aiguilles, elle est susceptible de guider ponctions, infiltrations et biopsies..
Les muscles
Les muscles normaux sont des structures striées composées de lignes hypoéchogè- nes parallèles (fibres musculaires) séparées par des lignes hyperéchogènes (squelette fibreux) qui se raccordent à angle aigu avec leur aponévrose (figure 2). Les pathologies musculaires traumatiques récentes (hématomes, désinsertions musculoaponévrotiques, ostéomes post-traumatiques) possèdent une expression échographique caractéristique (figures 2, 3). Les cicatrices se traduisent par une plage hyperéchogène localisée et les dégénérescences graisseuses par le remplacement de la structure hypoéchogène fibrillaire normale par une plage hyperéchogène diffuse (figure 4).

 3 a 3 b FIG. 3ab. — Choc direct (« béquille ») de la loge antérieure de la cuisse. a : coupe sagittale antérieure de la cuisse dix jours après le traumatisme : hématome juxta-osseux du muscle vaste intermé- diaire (astérisques), déjà en voie de calcification (flèches). b : le même jour, les calcifications sont à peine visibles en radiographie (flèches).
3 a 3 b FIG. 3ab. — Choc direct (« béquille ») de la loge antérieure de la cuisse. a : coupe sagittale antérieure de la cuisse dix jours après le traumatisme : hématome juxta-osseux du muscle vaste intermé- diaire (astérisques), déjà en voie de calcification (flèches). b : le même jour, les calcifications sont à peine visibles en radiographie (flèches).
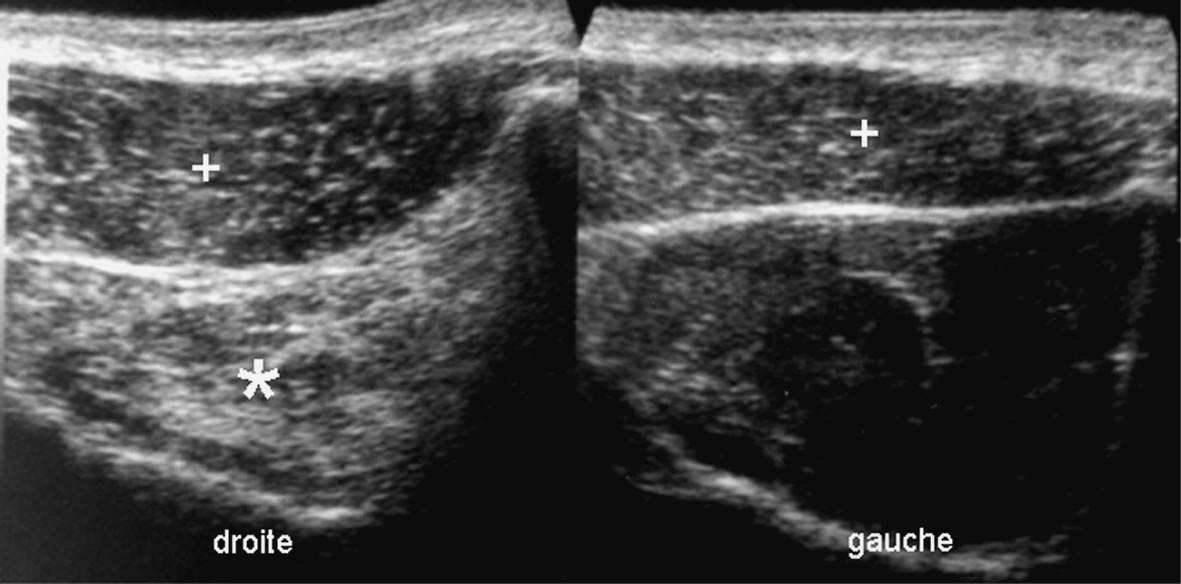

FIG. 4. — Dégénérescence graisseuse du muscle supra-épineux droit (astérisque) secondaire à une ancienne rupture transfixiante de son tendon. Le muscle droit est hyperéchogène par rapport au gauche, normal, et aux muscles trapèzes qui les recouvrent (+).
FIG. 5. — Images sémiologiques élémentaires des lésions tendineuses en échographie.
Les tendons
L’échographie est actuellement l’examen de première intention de la quasi-totalité des tendons de l’organisme, en particulier des tendons superficiels de l’épaule, du coude, de la main et du poignet, du genou, du pied et de la cheville. En coupe axiale, un tendon normal est une zone arrondie ou ovalaire, bien limitée, régulièrement semée de petits échos punctiformes qui lui donnent un aspect piqueté (figure 5). En coupe longitudinale, c’est une structure allongée, à bords nets et parallèles, soulignés par une fine ligne hyperéchogène dont le contenu, strié de fins échos linéaires parallèles au grand axe du tendon lui confère un aspect fibrillaire, hyperéchogène si les US abordent perpendiculairement le tendon (figure 5), hypoéchogène s’ils lui sont obliques : artéfact d’anisotropie. À l’état normal, il n’y a pas d’épanchement notable autour des tendons. La sémiologie des tendinopathies se résume à quelques lésions caractéristiques illustrées dans la figure 5. Ces aspects sémiologiques élémentaires donnent lieu à de multiples combinaisons et sont ainsi à l’origine d’un grand nombre d’images.
Les ligaments
Les ligaments normaux apparaissent tous sous forme d’une bande hyperéchogène fibrillaire et rectiligne s’ils sont mis en tension par des manœuvres adéquates [8] (figures 8 et 9). Les ligaments collatéraux des articulations superficielles, notamment ceux de la cheville et de l’arrière-pied, du genou, du coude, des doigts… sont actuellement individualisables. D’autres, plus délicats à explorer, sont en cours d’évaluation (ligaments du poignet, coraco-huméral, acromio-coracoïdien…).
Quant aux ligaments masqués par des structures osseuses (ligaments croisés du genou, ligament talo-calcanéen interosseux, ligament rond de la hanche) ils demeurent hors de portée de l’échographie.
La sémiologie échographique des entorses est simple. Une entorse bénigne se traduit par un ligament épaissi, hypoéchogène, qui perd son caractère strié, mais reste continu (figure 9). Dans l’entorse grave, le ligament est épaissi, hypoéchogène, interrompu en son corps ou à l’une de ses extrémités par une zone anéchogène, ou a une face superficielle concave (figure 10). L’arrachement d’une insertion osseuse correspond toujours une entorse grave. Toutes les entorses ne requièrent pas une échographie. Cet examen est justifié en cas de doute sur l’articulation en cause (par exemple articulations talo-crurale, sub-talienne ou médio-tarsienne), d’hésitation entre une entorse et une autre lésion dont le traitement est différent (lésion des ligaments fibulaires, fracture du processus latéral du talus…), de recherche d’une lésion associée à l’entorse (tendinopathie) ou en cas d’entorse chronique.

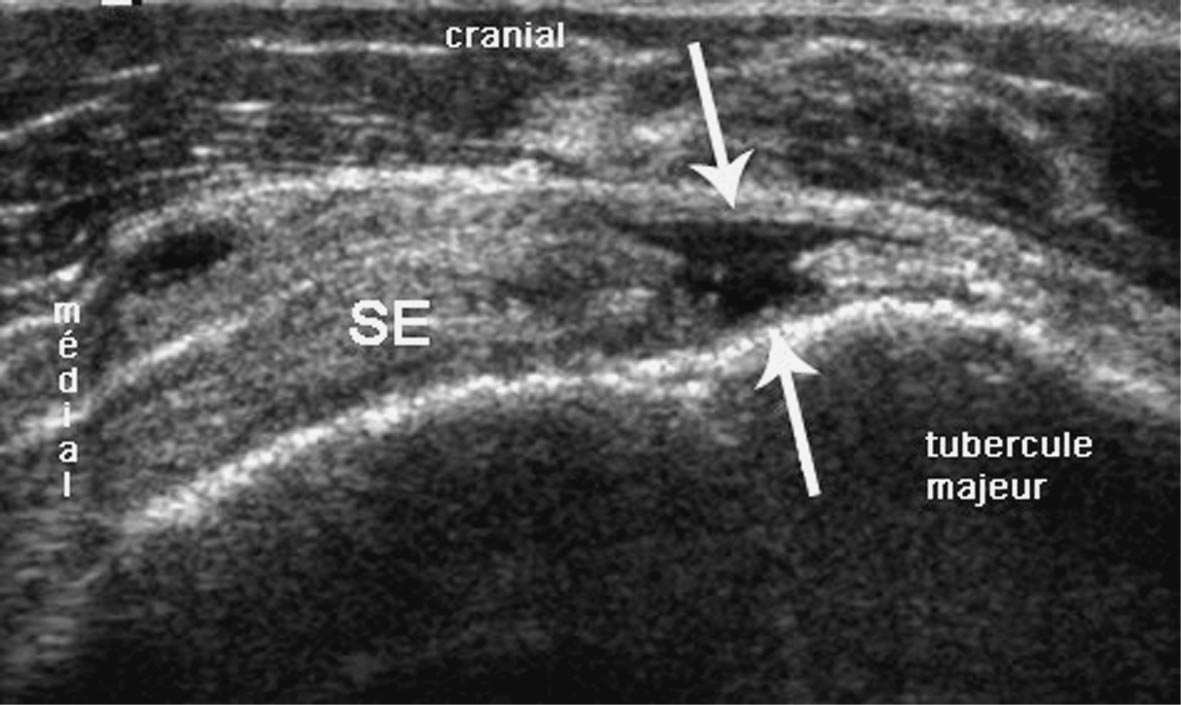 6 a 6 b FIG. 6ab. — a : Coupe axiale de la coulisse bicipitale. Elle est vide : le tendon du chef long du biceps est luxé médialement (flèche courbe), à la suite d’une rupture du tendon sub-scapulaire. b :
6 a 6 b FIG. 6ab. — a : Coupe axiale de la coulisse bicipitale. Elle est vide : le tendon du chef long du biceps est luxé médialement (flèche courbe), à la suite d’une rupture du tendon sub-scapulaire. b :
Coupe frontale du tendon supra-épineux (SE). Rupture transfixiante distale récente (flèches) emplie de liquide anéchogène.
Les nerfs
Tous les nerfs des membres sont explorables de façon détaillée, depuis la racine du membre (et même, pour le membre supérieur, depuis le plexus brachial) jusqu’à leurs branches distales millimétriques. L’un des atouts de l’échographie est la possibilité de suivre une structure linéaire (les nerfs en constituent un bon exemple) sur une grande longueur, de façon comparative. Guidée par l’examen clinique et l’électro-
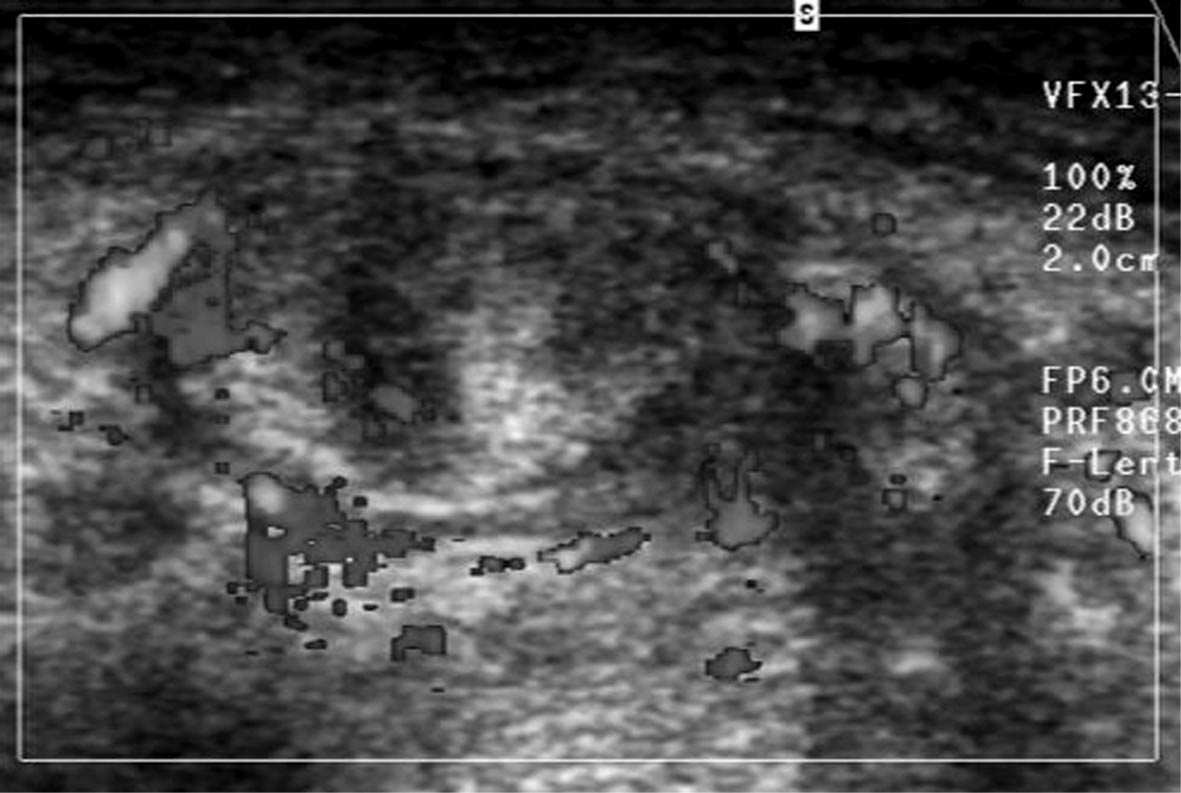 7 a 7 b FIG. 7ab. — Ténosynovite tibiale postérieure. a : Le tendon, dont le volume est augmenté, contient des plages hypoéchogènes (flèches). b : en Doppler puissance, hyperhémie intratendineuse et synoviale.
7 a 7 b FIG. 7ab. — Ténosynovite tibiale postérieure. a : Le tendon, dont le volume est augmenté, contient des plages hypoéchogènes (flèches). b : en Doppler puissance, hyperhémie intratendineuse et synoviale.
myogramme, l’échographie affirme la lésion d’un nerf, en détermine le niveau et en précise la nature : lésion traumatique, compression extrinsèque de différentes origines (syndrome canalaire, cal osseux, cicatrice, matériel d’ostéosynthèse..), tumeur (neurinome, neurofibrome..). Les syndromes canalaires les plus courants (compres-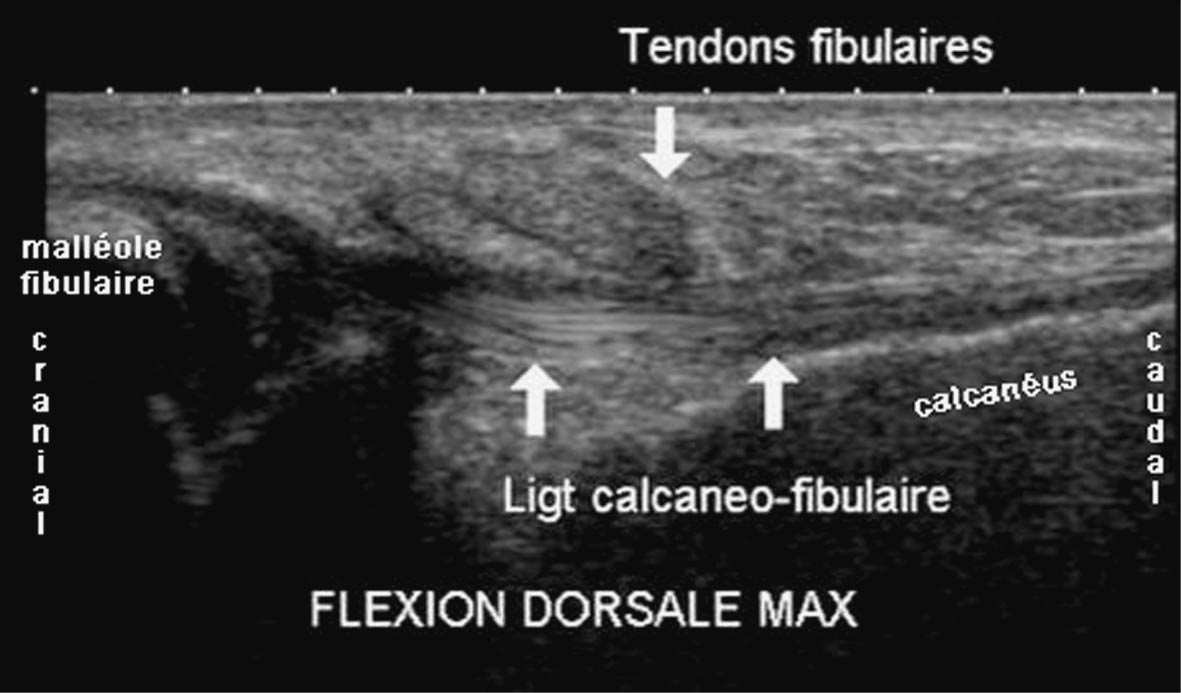
FIG. 8. — Ligament calcanéo-fibulaire normal, cheville en dorsiflexion. Dans cette position, le ligament (flèches) est tendu et soulève les tendons fibulaires qu’il écarte de la face latérale du calcanéus.
sion du nerf médian dans le canal carpien, du nerf ulnaire dans la loge de Guyon ou au coude [9], syndrome de Morton [10]) (figure 12)… bénéficient de cette méthode qui remplace progressivement l’IRM.
Les masses superficielles
La morphologie et la structure des tumeurs et pseudo-tumeurs peuvent être étudiées par l’échographie [11], suffisante lorsque l’image est absolument typique, par exemple celle d’un kyste mucoïde (figure 13), d’une bursite ou d’un lipome superficiel. En dehors de ces quelques cas typiques, a fortiori si la masse est solide, l’échographie doit céder le pas à l’IRM (technique plus sensible, qui couvre un champ plus vaste et étudie la vascularisation des tissus) et au besoin à la biopsie réglée.
Les corps étrangers
Qu’ils soient radio-opaques ou non, les corps étrangers des parties molles sont toujours bien visibles en échographie sous forme d’une image hyperéchogène. Dans certains cas leur exérèse peut être réalisée sous guidage échographique.
Les articulations
L’échographie met en évidence les épanchements intra-articulaires (figure 11), peu spécifiques sauf dans un contexte traumatique où la présence d’une hémarthrose et, plus encore, d’une lipohémarthrose, est très en faveur d’une fracture articulaire. Bien que le cartilage soit visible par endroits sous forme d’une bande hypoéchogène à la
 9 a 9 b FIG. 9ab. — Entorse bénigne du ligament talo-fibulaire antérieur droit. a : A gauche, le ligament normal est rectiligne et hyperéchogène (flèches). A droite, il est épaissi et hypoéchogène. Il demeure étanche, car l’épanchement sanguin (étoile) demeure intra-articulaire. b : en Doppler puissance, hyperhémie du ligament talo-fibulaire droit.
9 a 9 b FIG. 9ab. — Entorse bénigne du ligament talo-fibulaire antérieur droit. a : A gauche, le ligament normal est rectiligne et hyperéchogène (flèches). A droite, il est épaissi et hypoéchogène. Il demeure étanche, car l’épanchement sanguin (étoile) demeure intra-articulaire. b : en Doppler puissance, hyperhémie du ligament talo-fibulaire droit.
surface de l’os, il est hasardeux de tirer des conclusions quant à son état. Certains corps étrangers ostéochondromateux intra-articulaires sont visibles. L’échographie est un bon examen de certaines structures articulaires (membrane synoviale, capsule et ses renforcements ligamentaires, tendons adjacents, atmosphère périarticulaire…), mais ce n’est pas un examen de l’articulation dans sa globalité, en grande partie masquée par des reliefs osseux. Il existe quelques exceptions : les articulations des enfants dont les épiphyses, encore cartilagineuses, sont mal analysables par la radiographie. Il en est ainsi de la hanche du nouveau-né, pour laquelle l’échographie est l’examen de choix, des malformations des pieds du nourrisson, des synchondroses non visibles à la radiographie.
Les prothèses articulaires (prothèse totale de hanche, du genou..) où la présence de matériel gêne considérablement l’IRM et la tomodensitométrie, bénéficient, également en cas de complications, de l’échographie, peu handicapée par le métal.
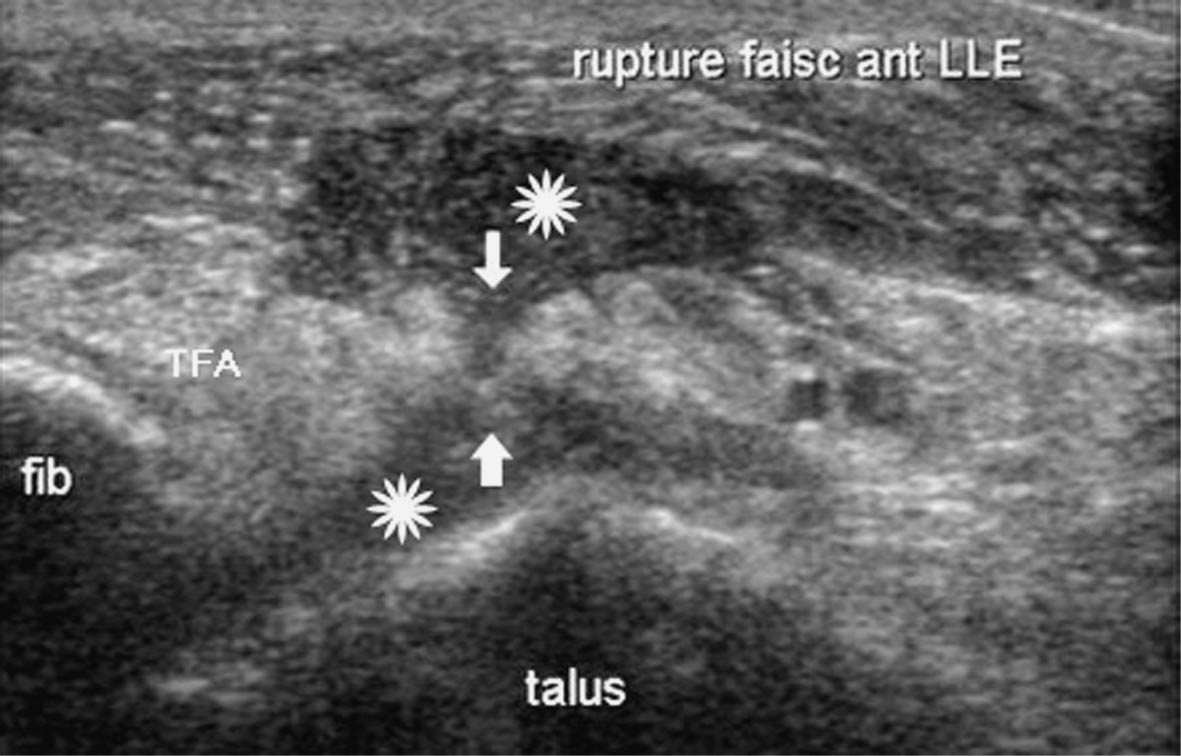
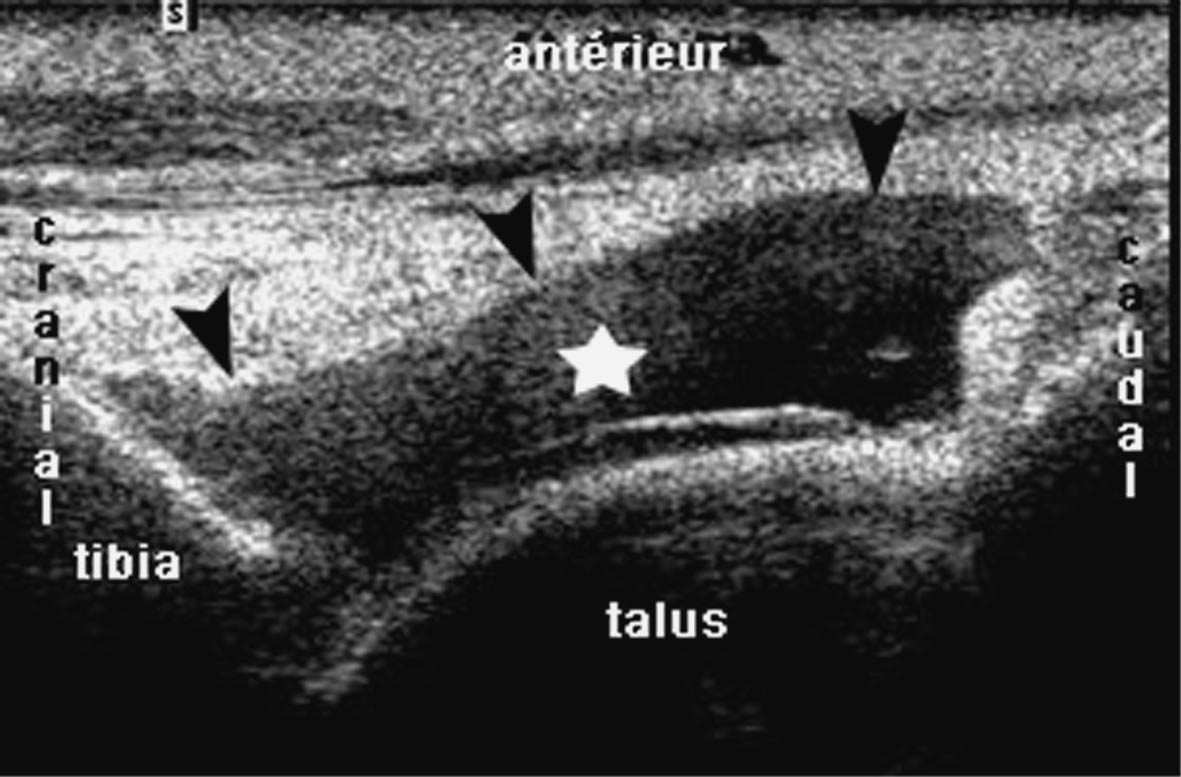
FIG. 10. — Entorse grave du ligament talo-fibulaire antérieur. Rupture transfixiante du corps du ligament (flèches) par où s’échappe l’épanchement intra-articulaire (étoiles).
FIG. 11. — Épanchement de l’articulation talo-crurale (étoile) : plage hypoéchogène bien limitée (têtes de flèches) qui distend le récessus antérieur de l’articulation.
La surface des os
Elle est parfaitement analysable en échographie, qui décèle précocement, alors que la radiographie est encore normale, un hématome sous-périosté témoin d’une fracture de fatigue (figure 14), un abcès secondaire à une ostéomyélite, une petite marche d’escalier signe d’une fracture, la saillie anormale d’un cal osseux, d’un matériel prothétique ou d’ostéosynthèse…
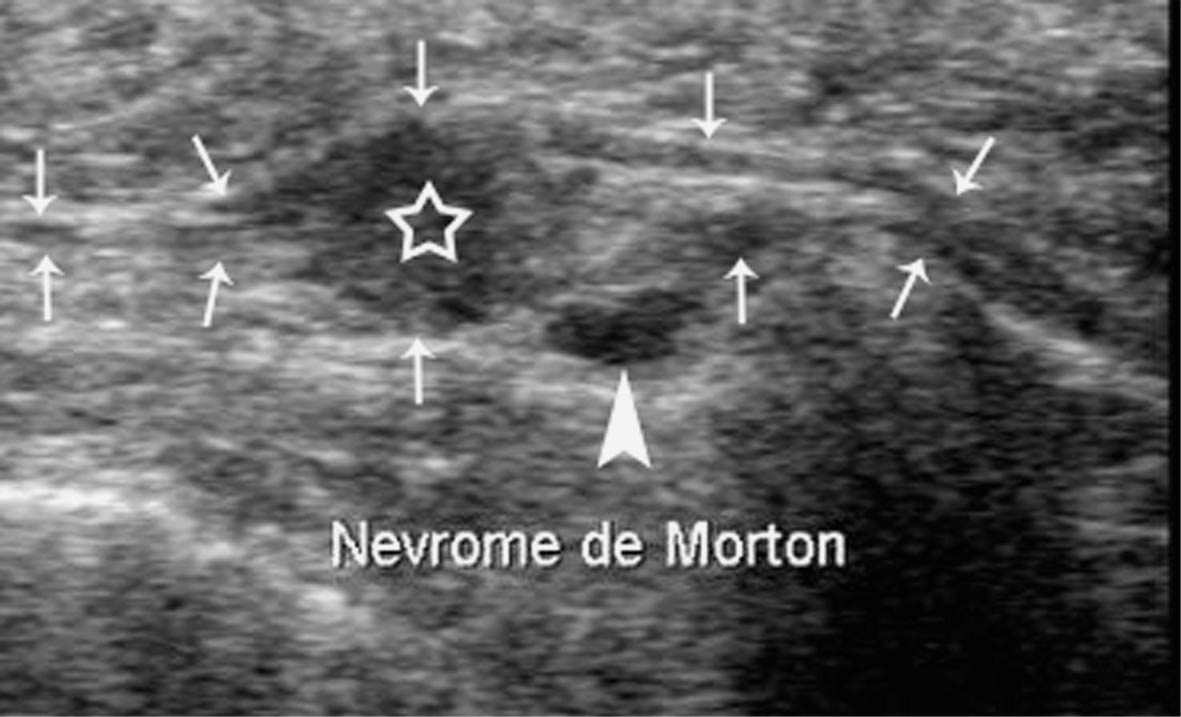
FIG. 12. — Névrome de Morton (étoile). Il se raccorde avec le nerf en aval et en amont (flèches) et est accompagné par une petite bursite sentinelle (tête de flèche).
Les ponctions sous guidage échographique
L’échographie visualise en temps réel la progression d’une aiguille et peut guider l’évacuation d’un hématome ou d’un abcès, l’infiltration d’un dérivé corticoïde, l’ablation d’un corps étranger, une ponction-biopsie… Ces manœuvres nécessitent de strictes mesures d’asepsie [8), plus difficiles à respecter qu’en radiographie ou en scanner, compte tenu de la proximité de la sonde et de l’aiguille de ponction, ainsi que de la présence du gel…
INCONVÉNIENTS DE LA MÉTHODE
Ce sont essentiellement la longueur et la difficulté de la courbe d’apprentissage, la cotation des examens, le coût des équipements et la transmission des dossiers.
Pour être performant en échographie de l’appareil moteur il est nécessaire de mettre à jour ou d’acquérir, puis d’entretenir, des connaissances anatomiques approfondies (qui ne font pas partie du cursus radiologique habituel), de connaître la clinique, d’avoir de bonnes bases d’anatomopathologie macroscopique, et si possible d’avoir pratiqué l’IRM et la TDM, excellents « professeurs » d’échographie. La souscotation des examens et le prix élevé des appareils d’échographie perfectionnés, indispensables à cette pratique, ne favorisent guère la diffusion de l’échographie de l’appareil moteur, grande consommatrice de temps-médecin. Enfin, la fréquente méconnaissance d’un élément essentiel : la transmission du message au clinicien, sous forme d’images-clefs caractéristiques, compréhensibles, annotées, orientées, exploitables d’un point de vue thérapeutique, explique certains rejets de la part des cliniciens.

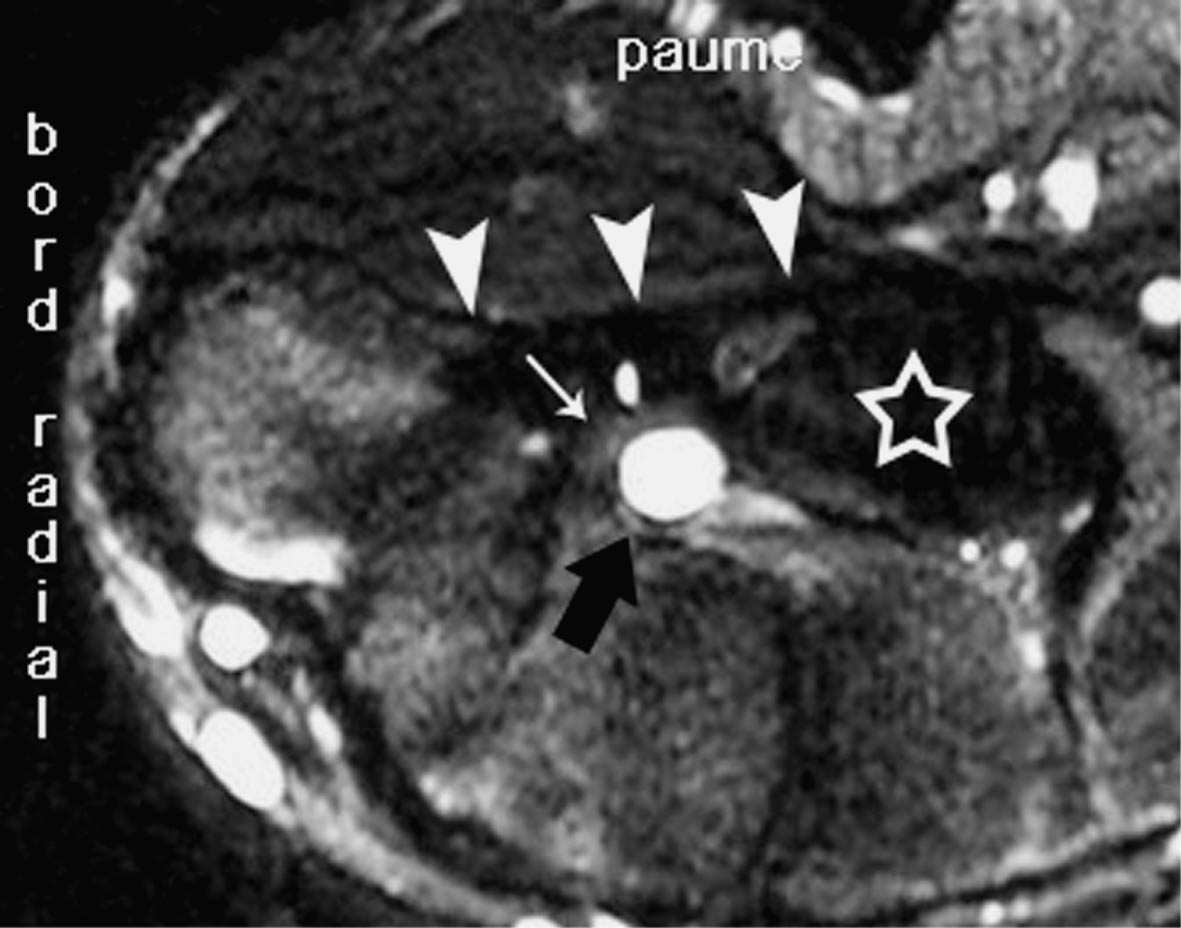 13 a 13 b FIG. 13ab. — Kyste mucoïde du canal carpien (grosse flèche). Il comprime le tendon long fléchisseur du pouce (petite flèche) contre le rétinaculum des fléchisseurs (têtes de flèches). Les autres tendons sont repérés par une étoile. a : coupe échographique. b : même coupe en IRM pondérée en T2.
13 a 13 b FIG. 13ab. — Kyste mucoïde du canal carpien (grosse flèche). Il comprime le tendon long fléchisseur du pouce (petite flèche) contre le rétinaculum des fléchisseurs (têtes de flèches). Les autres tendons sont repérés par une étoile. a : coupe échographique. b : même coupe en IRM pondérée en T2.
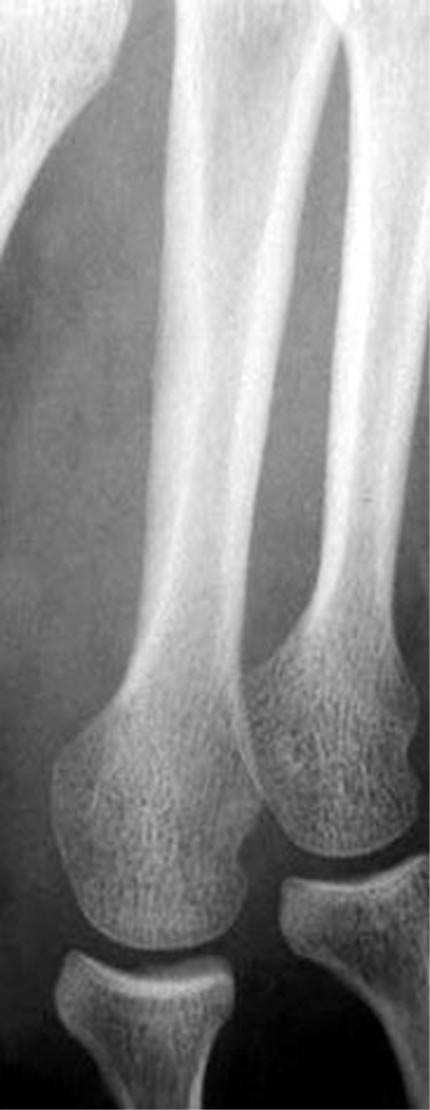
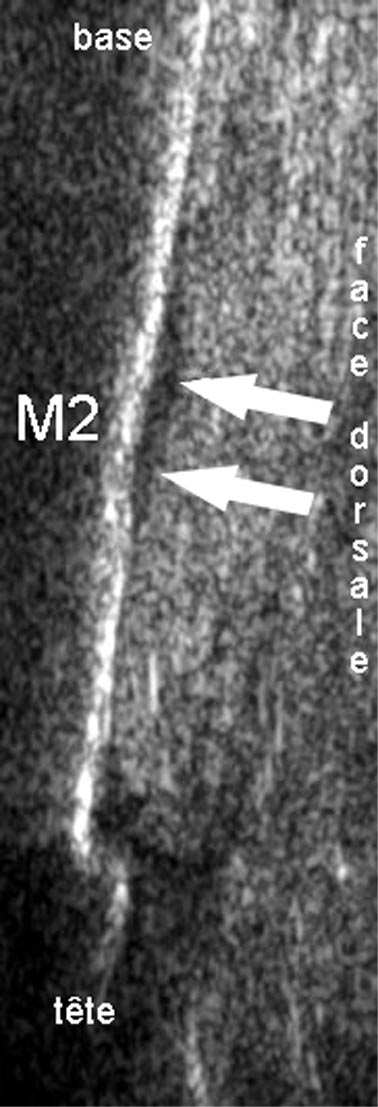 14 a 14 b FIG. 14ab. — Fracture de fatigue diaphysaire du deuxième métatarsien datant de trois jours. a :
14 a 14 b FIG. 14ab. — Fracture de fatigue diaphysaire du deuxième métatarsien datant de trois jours. a :
radiographie normale. b : coupe échographique : hématome sous-périosté (flèches). La radiographie est devenue pathologique huit jours après.
CONCLUSION
Une des grandes faiblesses de la radiographie conventionnelle est son impuissance à analyser les parties molles. La TDM, et surtout l’IRM, y parviennent, mais à un prix de moins en moins compatible avec les contraintes de plus en plus rudes qui pèsent actuellement sur le système de santé. L’échographie, technique jeune et encore en pleine évolution, apporte une solution alternative très actuelle, servie par une innocuité totale, une accessibilité inégalée, un coût imbattable (15 fois moins lourd qu’un examen IRM) et une faculté unique d’étude des structures en mouvement.
L’étude des parties molles ne représente qu’un aspect particulier d’une tendance plus générale : pour de nombreux spécialistes qu’ils soient radiologistes, urgentistes, gastroentérologues, cardiologues, obstétriciens, chirurgiens… les US sont devenus une technique quotidienne indispensable, prioritaire, pour laquelle de nouvelles indications apparaissent tous les jours. À ce titre, le développement et la promotion de cette technique mériteraient un soutien actif de la part de nos instances décisionnaires.
BIBLIOGRAPHIE [1] INADA G., ISHIZAKI M. — Comparative studies on x-ray and ultrasound diagnosis of cross section images of human limbs. Nagoya. Med. J. , 1969, 15 , 19-21.
[2] OKSALA A., HAKKINEN L. — Comparative experiments on the attenuation of ultrasound in muscular and fat tissue. Acta. Ophtalmol., (Copenh), 1969, 47 , 739-742.
[3] MOORE C.P., SARTI D.A., LOUIE J.S. — Ultrasonographic demonstration of popliteal cyst in rheumatoid arthritis. Arthritis Rheum , 1975, 18 , 557-580.
[4] FORNAGE B. — Echographie du système musculo-tendineux des membres. Atlas d’anatomie ultrasonore normale. (Vigot Édit., Paris), 1987.
[5] GHOZLAN C., GODEFROY D., PALLARDY G. — L’échographie dans l’exploration des parties molles des membres : étude de 200 dossiers. JEMU , 1983, 4 , 195-203.
[6] MORVAN G. — L’échographie du système locomoteur.
J. Radiol. , 1989, 70 , 513-527.
[7] BARNETT S.B., ter HAAR G.R., ZISKIN M.C., ROTT H.D., DUCK F.A., MAEDA K. — International recommandations and guidelines for the safe use of diagnostic ultrasound in medicine.
Ultrasound in Med and Biol , 2000, 26 , 355-366.
[8] BRASSEUR J.L., TARDIEU M. — Échographie du système locomoteur. (Masson Édit., Paris), 1998.
[9] BRASSEUR J.L., JACOB D., CRETEUR V., COURTHALIAC C., BARGOIN R., SASSUS B. et al. —
Sonoanatomy of the ulnar nerve in the cubital tunnel : a multicentre study by the GEL.
Eur.
Radiol , 2004, 14 , 1170-1773.
[10] MORVAN G., MATHIEU P., BUSSON J., WYBIER M. — L’imagerie du névrome de Morton.
In « Imagerie du pied et de la cheville », sous la coordination de CHEVROT A., MORVAN G.,
DIEBOLD P., EULRY F., BENAMOU P., JARDE O. ET al. GETROA opus XXIX, (Sauramps
Médical, Montpellier, Édit.), 2002, 127-136.
[11] BRASSEUR J.L., ZEITOUN D., DION E. — Place et limites de l’échographie en cas de tumeur des parties molles. In « Conduite à tenir devant une image osseuse ou des parties molles d’allure tumorale » sous la coordination de LAREDO J.D., TOMENO B., MALGHEM J., DRAPE J.L., WYBIER
M., RAILHAC J.J., GETROA opus XXXI, (Sauramps Médical, Montpellier, Édit.), 2004, 297-312.
DISCUSSION
M. Louis AUQUIER
Quelle est la relation des constatations anatomiques que permet l’échographie avec l’élé- ment douleur qui constitue le plus souvent le premier sujet d’appel dans cette pathologie ? Et au-delà, ne faudrait-il pas faire une étude comparative des images constatées aux différents âges de la vie ?
Cette question aborde le point crucial de toute l’imagerie : le décalage entre morphologie et symptomatologie. Comme toutes les techniques d’imagerie, l’échographie, est un examen complémentaire de l’examen clinique, lui-même motivé par une plainte du patient, souvent la douleur. Elle ne concerne donc, par définition, que les patients symptomatiques. L’étude de patients asymptomatiques a montré que le vieillissement de
nos structures anatomiques, traduit par des remaniements morphologiques d’intensité variable, n’est que très inconstamment corrélé à une symptomatologie douloureuse. Une hyperhémie, visible à l’écho Doppler, serait l’un des signes les plus fréquemment corrélé à la douleur.
M. Michel ARTHUIS
Est-il possible d’étudier l’aponévrose plantaire pour expliquer la talalgie des adolescents sportifs ?
Oui. L’échographie met facilement en évidence les remaniements de l’aponévrose plantaire qu’ils siègent à son insertion ou en son corps. Elle constitue actuellement l’imagerie de base de cette structure. Cependant, une inflammation purement intra-osseuse, comme dans certaines spondylarthropathies débutantes de l’adolescent, est invisible en échographie. Suspectée sur la scintigraphie, elle n’apparaît qu’en IRM.
M. Jean DUBOUSSET
Avez-vous tenté de faire des échographies circulaires du genou pour étudier les ménisques ?
Pouvez-vous apprécier l’évolution des traumatismes chirurgicaux ou autre des tendons et leur cicatrisation ?
Oui, mais ce fût un échec. Les ultrasons, arrêtés par l’os, ne peuvent aborder les ménisques du genou en totalité. Dans certains cas ils peuvent, au mieux, faire soupçonner une fissure périphérique de ces derniers mais sont par contre très performants dans la mise en évidence des kystes méniscaux périphériques. L’augmentation de volume d’un tendon opéré est normale. La détection échographique d’une collection intra ou péritendineuse est un élément de mauvais pronostic. Il semble en être de même de la persistance d’une hypervascularisation péritendineuse et la présence d’un flux intratendineux de type résistif au Doppler pulsé après quelques mois.
M. Charles-Joël MENKÈS
Quelle est la valeur de l’échographie pour dépister les corps étrangers intra-articulaires de l’ostéochondromatose à la hanche et au genou ? Pour l’épaule, l’IRM n’est-elle pas supé- rieure à l’échographie ?
L’échographie détecte facilement les corps étrangers intra-articulaires dans la mesure où ceux-ci siègent dans une région accessible aux ultrasons. C’est le cas au genou, où ils sont le plus souvent rassemblés dans le cul-de-sac sous-quadricipital ou dans la partie postérieure de l’échancrure inter-condylienne. À la hanche, les corps étrangers péricervicaux sont visibles, mais ceux de l’arrière-fond du cotyle échappent aux ultrasons, tandis qu’à l’épaule, ceux de la coulisse bicipitale apparaissent à l’évidence, mais ceux qui siègent dans le récessus sous-coracoïdien sont masqués par le processus coracoïde.
L’examen de référence des corps étrangers intra-articulaires quelle qu’en soit l’origine demeure l’arthro-scanner, plus performant que l’IRM.
M. Philippe VICHARD
Je m’interroge sur la place de l’échographie parmi les indications d’examens complémentaires. En effet, cette échographie peut être considérée comme un prolongement de l’examen clinique mais elle est souvent surclassée par le scanner et l’IRM, de sorte que l’on peut se demander s’il ne faut pas recourir d’emblée à l’examen de référence. Dans ce schéma, l’échographie devient une source de majoration des coûts. Recourir à l’échographie pour une contusion des parties molles, une rupture tendineuse, un hygroma, ou une entorse ne me paraît pas judicieux. Et, mise à part la luxation congénitale du nourrisson, à dépister, je ne vois guère que les néoformations sur les trajets nerveux qui illustrent l’intérêt spécifique de l’échographie, en chirurgie orthopédique. Ma question concernera aussi la maladie de Morton : la localisation des névromes, si utile avant d’opérer par un abord limité, est-elle plus performante qu’avec l’IRM ?
De l’avis général, à l’heure actuelle, les performances de l’échographie dans nombre de pathologies orthopédiques courantes des parties molles : pathologies tendineuses, ligamentaires, musculaires, nerveuses… approchent ou égalent celles de l’IRM et sont nettement supérieures à celles du scanner pour un coût minime, une irradiation nulle et une grande disponibilité. L’examen clinique, même réalisé par un orthopédiste compé- tent, n’étant pas infaillible pourquoi, en cas de besoin, réfuter cet examen complémentaire ? L’exemple du névrome de Morton est particulièrement édifiant : en diagnostiquant et en localisant le ou les névromes dans plus de 85 % des cas, l’échographie autorise, sans risque d’erreur de diagnostic ou d’espace, un abord chirurgical dorsal peu traumatisant de l’avant-pied.
M. Claude DREUX
L’échographie pourrait-elle permettre un meilleur dépistage de l’ostéoporose par l’ostéodensitométrie ? Des méthodes dites « aux ultrasons » sont très utilisées aux USA notamment au niveau du calcanéus. Une échographie au niveau de la hanche ou du poignet aurait-elle un intérêt ?
La densitométrie échographique commence à être utilisée au niveau du calcanéus et est encore à l’état de recherche au niveau du col du fémur et du poignet. Des études en cours devraient permettre de juger de la reproductibilité et de la fiabilité de ces dernières mesures. Actuellement, l’absorptiométrie biphotonique à rayons X reste cependant le seul standard reconnu par les critères de définition de la maladie selon l’Organisation Mondiale de la Santé.
M. Yves CHAPUIS
Ma première question a trait au caractère opérateur dépendant de l’examen. Pouvez-vous commenter ce point ? La seconde est liée au difficile problème de la formation. Où en êtes-vous ? Pensez-vous par ailleurs que l’échographie telle que vous la pratiquez puisse faire l’objet d’une délégation de compétence à un personnel paramédical ?
Votre question est triple. — Les performances de l’échographie dépendent effectivement de la qualité de l’opérateur, ce qui est d’ailleurs le cas d’une grande partie de la médecine :
acte chirurgical, endoscopie, voire simple consultation… Elles dépendent aussi du maté-
riel utilisé. De bons résultats impliquent l’utilisation d’un matériel performant mais coûteux. — La formation théorique et pratique des médecins n’est que partiellement résolue. Les connaissances anatomiques, anatomopathologiques et cliniques approfondies indispensables sont longues à acquérir. Comme pour la chirurgie, la réalisation pratique des échographies ne s’apprend que par compagnonnage, technique lente qui demande de nombreux formateurs de qualité. Actuellement la formation est assurée par des filières universitaires et post-universitaires, encore insuffisantes et des sociétés savantes telles le GEL (Groupe des Échographistes Locomoteurs) qui organisent congrès et ateliers. Nous manquons de terrains de stage et de formations adaptées aux cliniciens. — Il parait dans l’avenir, inévitable, vu la pénurie de médecins spécialisés, de déléguer certaines tâches échographiques au personnel paramédical. Si une délégation globale parait irréaliste, compte tenu de la complexité de la méthode, des délégations spécifiques, sous contrôle médical strict, et après formation complémentaire appropriée, sont envisageables.
M. Pierre GODEAU
Quel est l’apport de l’échographie pour le diagnostic de PPR ?
Le diagnostic de la pseudo-polyarthrite rhizomélique demeure clinique et biologique.
L’écho Doppler peut mettre en évidence des signes d’artérite temporale qui font craindre une maladie de Horton. Un épanchement bilatéral de la bourse séreuse sous-acromiodeltoïdienne serait un signe sensible et spécifique en faveur du diagnostic de PPR.
M. Bernard SALLE
L’échographie des hanches chez le nouveau-né est-elle fiable à 100 % pour le dépistage de la luxation congénitale ?
Malgré son manque de totale fiabilité (de 0,5 à 1 pour 1.000 enfants sont mal évalués malgré un examen correct) l’examen clinique à la naissance reste à la base du dépistage de la maladie luxante de la hanche. En cas de doute clinique, l’échographie a été reconnue par une Conférence de Consensus comme un examen fiable pour classer initialement la hanche en normale, pathologique ou douteuse, et suivre éventuellement son évolution sous traitement.
M. Jean-Baptiste PAOLAGGI
Il manque une étude chez des sujets asymptomatiques car il est indispensable de connaître la fréquence des faux-positifs. Quelle est la place de l’échographie dans l’exploration du creux poplité et en particulier pour différencier compression veineuse par kyste et thrombophlébite et éviter ainsi des traitements injustifiés ?
L’échographie est actuellement l’examen de référence dans l’étude du creux poplité. Elle permet avec certitude le diagnostic de kyste poplité, rompu ou non, avec ou sans compression de la veine poplitée et, aidée de l’écho Doppler, d’une éventuelle phlébite poplitée.
M. Paul DOURY
En matière de fracture de fatigue au stade précédant la fracture, c’est-à-dire au stade douloureux correspondant à l’œdème intra-osseux, la scintigraphie osseuse ou l’IRM ne sont-elles pas supérieures à l’échographie ?
Indiscutablement. L’IRM, aussi sensible que la scintigraphie, mais plus spécifique (bien que cette dernière puisse souvent donner des images très évocatrices) est plus sensible et plus spécifique que l’échographie. Cependant, surtout dans les sites anatomiques facilement accessibles, en cas de contexte clinique évocateur, la mise en évidence échographique d’un hématome sous-périosté apporte un argument de poids au diagnostic et permet de mettre en route un traitement adapté, sans attendre l’apparition des signes radiographiques classiques.
M. Bernard GLORION
L’orateur a demandé la performance obtenue par la radio du bassin. Celle-ci a été supprimée au bénéfice de l’échographie.
L’examen clinique néonatal, complété en cas de doute par une échographie, permet de classer les hanches des nouveau-nés en normales, pathologiques ou douteuses, et de réserver une éventuelle radiographie à trois mois aux quelques cas pathologiques ou douteux qui en ont réellement besoin, ce qui limite l’irradiation de la population fragile des nouveau-nés.
M. Jean Daniel PICARD
Vous n’avez pas parlé des éventuelles complications de l’échographie. Pouvez-vous apporter quelques commentaires dans ce domaine et plus particulièrement nous préciser les éventuelles complications des produits de contraste dont l’utilisation constitue une importante voie de recherche ?
Les ultrasons entraînent une augmentation de chaleur (mesurée par l’index thermique) et de pression (mesurée par l’index mécanique). À l’heure actuelle, il n’a été rapporté, à notre connaissance, aucune complication des ultrasons utilisés à visée diagnostique dans l’exploration des parties molles. Toutefois, des lésions tissulaires pulmonaires ont été prouvées expérimentalement pour des puissances voisines de celles utilisées en clinique.
La prudence consiste donc à limiter le temps d’exposition aux ultrasons et la puissance des machines à ce qui est réellement utile au diagnostic. Les produits de contraste ne sont pas, à l’heure actuelle, communément utilisés dans l’exploration des parties molles et, à notre connaissance, aucune complication n’a pu leur être imputée dans ce domaine.
* Gérard MORVAN, Cabinet d’Imagerie de l’Appareil Moteur. 5, rue Alfred Bruneau. 75016 Paris. ** Jean Louis BRASSEUR, 33, rue Paul Bert, 93370 Montfermeil. *** Groupe des Échographistes de l’appareil Locomoteur (GEL). 80, avenue Félix Faure, 75015 Paris. Tirés-à-part : Monsieur le Docteur Gérard MORVAN, même adresse. Article reçu le 7 février 2005, accepté le 28 février 2005.
Bull. Acad. Natle Méd., 2005, 189, no 4, 675-696, séance du 12 avril 2005


