Résumé
La cystectomie radicale est le traitement de référence du cancer infiltrant de vessie non métastatique. Aujourd’hui, la majorité des patients bénéficient d’une entéroplastie de substitution après cystectomie. La dérivation trans-iléale de Bricker est réservée aux patients ayant un cancer envahissant l’urètre, aux patients d’un âge avancé, et aux femmes qui sont à haut risque d’incontinence urinaire sévère après entéroplastie. Grâce aux progrès de l’anesthésie, des techniques chirurgicales, et de la réanimation, la cystectomie radicale avec entéroplastie de substitution est aujourd’hui réalisée en pratique courante. Pour les cancers localisés à la vessie (stade T2N0M0), elle est associée à un taux de survie sans récidive à 10 ans d’environ 80 %. Les complications précoces, qui surviennent chez moins de 30 % des opérés, sont essentiellement médicales : troubles cardio-vasculaires, embolie pulmonaire, désorientation temporo-spatiale, infections urinaires et pulmomaires sont les plus fréquentes. Les complications tardives, plus rares, sont surtout chirurgicales : sténose des anastomoses urétéro-iléales, sténose de l’anastomose urétro-néovésicale, et occlusion du grêle.
Summary
Radical cystectomy is the standard treatment for muscle-invasive bladder cancer. Today, most patients can undergo substitution enteroplasty following cystectomy. Recto-colic urinary diversions and cutaneous ureterostomy are now uncommon. An ileal conduit (Bricker) may be proposed to patients with urethral involvement, as well as to elderly patients and to women who are at a high risk of severe urine leakage following enteroplasty. Thanks to progress in anesthesia, surgical techniques and intensive care, cystectomy with substitution enteroplasty is now a routine procedure. For localized bladder cancer (pT2N0M0 stage), this intervention is associated with a 10-year survival rate of about 80 %. The mean length of stay in the intensive care unit varies between 1 and 7 days, and the mean total hospital stay ranges from 10 to 13 days. Early complications, which occur in less than 30 % of cases, are mainly medical ; the most common are cardiovascular complications, pulmonary embolism, disorientation and urinary tract and pulmonary infections. Late complications are less common and are mainly surgical ; they include uretero-ileal stenoses ( ∼ 10 % of cases), uretero-ileal stenosis (4 %), and intestinal obstruction (4 %). Urinary and sexual disorders are frequent after radical cystectomy and substitution enteroplasty. Early postoperative incontinence occurs in more than 50 % of cases but often responds to physiotherapy. In contrast, most male patients remain impotent. Simple transurethral resection of the prostate with cystectomy may be used instead of radical cystoprostatectomy in order to reduce the risks of incontinence and impotence, but this approach is controversial, as some authors have reported an increased risk of recurrence and metastasis.
INTRODUCTION
En fréquence, le cancer de la vessie se situe au 9ème rang de l’ensemble des cancers.
En l’an 2000, son incidence dans le monde était estimée à 336.000 nouveaux cas par an [1]. L’incidence du cancer de la vessie est croissante. En France, son incidence augmente d’environ 1 % par an. En Europe et aux États-Unis, le type histologique le plus fréquent est le cancer urothélial, qui représente plus de 90 % des variantes de tumeur vésicale. Le facteur de risque principal du cancer urothélial est le tabac. Plus rarement, le cancer urothélial est favorisé par une exposition professionnelle à certains agents, dont les amines aromatiques et les hydrocarbures. Dans certains pays d’Afrique, le type histologique prédominant est le cancer épidermoïde, qui est favorisé par la Bilharziose.
Le diagnostic histologique et le stade de la tumeur sont établis par résection trans-uréthrale. Les tumeurs superficielles Ta, T1, et le carcinome in situ sont traités par résection trans-uréthrale plus ou moins suivie d’instillations endo-vésicales. Les tumeurs T2, qui infiltrent la musculaire, nécessitent un traitement plus lourd. En cas d’envahissement ganglionnaire et/ou de métastases à distance, ces tumeurs relèvent de la chimiothérapie. En l’absence d’extension extra-vésicale, le traitement de référence est la cystectomie radicale.
Ces 20 dernières années, les taux de mortalité et de morbidité après cystectomie radicale ont considérablement baissé. Aujourd’hui, ces taux respectifs sont infé- rieurs à 3 % et 30 % [2]. Dans les études récentes, la cystectomie permet un taux de survie sans récidive à 10 ans supérieur à 80 % lorsque la maladie est limitée à la paroi vésicale [3]. D’autre part, les modes de dérivation urinaire ont beaucoup changé.
L’urétérostomie cutanée et la dérivation colique ou rectale des uretères sont très rarement utilisées. La dérivation trans-iléale de Bricker garde certaines indications, en particulier les patients âgés et les femmes. L’entéroplastie de substitution est aujourd’hui réalisée dans la plupart des cas ; elle permet d’éviter une stomie. Ses résultats carcinologiques sont satisfaisants, et sa morbidité est acceptable.
Indications de la cystectomie radicale
Le traitement du cancer infiltrant de vessie dépend de son extension. Le bilan d’extension repose sur le scanner thoraco-abdomino-pelvien. Une scintigraphie osseuse est justifiée seulement en cas de point d’appel clinique.
En cas d’adénopathies pelviennes ou lombo-aortiques isolées, le traitement de référence est la chimiothérapie (association gemcitabine + cisplatine). S’il existe une réponse complète à la chimiothérapie, une cystectomie dite de « sauvetage » peut être envisagée. Le bénéfice de la cystectomie de sauvetage est controversé, car le taux de survie à 5 ans est inférieur à 30 % [4].
En cas de métastases à distance, la cystectomie n’a aucun bénéfice carcinologique.
Dans de rares cas, elle peut être indiquée à visée symptomatique. En effet, certains patients ont des troubles mictionnels très invalidants liés à leur tumeur vésicale, ou des hématuries répétées occasionnant des hospitalisations fréquentes pour transfusion. Une cystectomie peut donc être proposée à ces patients, uniquement dans le but d’améliorer leur qualité de vie.
Enfin, lorsque le bilan d’extension est négatif, le traitement de référence est la cystectomie radicale. Celle-ci consiste en une cysto-prostatectomie chez l’homme, ou en une pelvectomie antérieure chez la femme. L’âge supérieur à 75 ans ne représente plus, en soit, une contre-indication à la cystectomie. Des études récentes ont montré que dans cette population, la cystectomie avait des taux de mortalité et de morbidité similaires à ceux de la population plus jeune [5]. En revanche, chez les patients qui ont une espérance de vie courte en raison d’un âge très avancé et/ou de co-morbidités sévères, la cystectomie est contre-indiquée. Le traitement repose alors sur des résections trans-uréthrales itératives.
Modes de dérivation urinaire et de reconstruction après cystectomie
L’urétérostomie cutanée
L’urétérostomie cutanée est devenue exceptionnelle. Ses indications sont limitées aux patients fragiles, chez qui il est risqué d’envisager des sutures digestives : patients très âgés, lésions radiques intra-péritonéales, antécédents multiples de chirurgie abdominale. L’urétérostomie cutanée, autrefois très utilisée, a été quasiment abandonnée en raison de son caractère contraignant (présence de deux poches urinaires), et de la fréquence des sténoses des anastomoses urétéro-cutanées.
Les dérivations coliques ou rectales
La dérivation colique ou rectale est également très rarement utilisée. L’intervention de Coffey, qui consiste à aboucher les uretères dans le rectum, se complique quasi constamment de pyélonéphrites par reflux [6]. Elle occasionne également des troubles métaboliques, et induit un risque tumoral. Dans les séries historiques, cette technique se compliquait d’insuffisance rénale dans 30 % des cas. La confection
d’un réservoir sigmoïdien est moins morbide. La poche de Mayence est une anse sigmoïdienne détubulée, sur laquelle sont abouchés les uretères. La création d’un réservoir à basse pression supprime, en théorie, le risque de reflux et de pyélonéphrites [7].Cependant, cette technique a un taux de morbidité non négligeable, et altère significativement la qualité de vie des patients qui acceptent difficilement le fait d’uriner par l’anus. En conséquence, la dérivation colique ou rectale après cystectomie n’est quasiment plus utilisée. Ses seules indications sont l’existence d’un grêle court ou de lésions radiques du grêle, qui rendent impossible l’utilisation d’un greffon iléal.
Les dérivations cutanées continentes
Plusieurs techniques de dérivation cutanée continente ont été décrites, la plus connue étant la poche de Kock [6]. Un segment iléal d’environ 80 cm est prélevé. Un réservoir est réalisé en plicaturant l’anse en forme de U. Les uretères sont anastomosés à l’extrémité d’un jambage. L’autre extrémité est invaginée par plusieurs rangées d’agrafes, puis extériorisée soit dans la fosse iliaque, soit dans l’ombilic.
Lorsque l’urine s’accumule dans le réservoir, elle fait pression sur l’extrémité distale invaginée, ce qui assure la continence. Les mictions se font par auto-sondages. Alors que les dérivations cutanées continentes sont relativement courantes aux ÉtatsUnis, elles sont très peu utilisées en France. Les complications sont fréquentes :
difficultés de cathétérisation, désinvagination de la stomie, et formation de calculs à long terme (10 % des cas).
La dérivation trans-iléale de Bricker
La dérivation de Bricker consiste à prélever un greffon iléal d’environ 20 cm. Les deux uretères sont abouchés à une extrémité du greffon. L’autre extrémité est directement abouchée à la peau. L’avantage de cette technique est le faible taux de complications spécifiques. En dehors des complications relatives à toute cystectomie, les deux complications précoces du Bricker sont la fistule iléo-iléale (< 5 % des cas) et la fistule urétéro-iléale (< 5 % des cas). À distance, les deux complications principales sont les sténoses des anastomoses urétéro-iléales (10 % des cas), et le prolapsus de la stomie (10 % des cas) [8]. Le problème principal est la présence d’une poche, qui nécessite un appareillage quotidien. Pour cette raison, la dérivation de Bricker est réservée aux patients qui ont une contre-indication à l’entéroplastie de substitution : patients ayant une tumeur envahissant l’urèthre (risque de récidive pelvienne nécessitant une radiothérapie adjuvante), et patients très âgés qui sont à haut risque d’incontinence sévère après entéroplastie. Pour la plupart des équipes, une dérivation de Bricker est systématiquement réalisée chez les femmes. En effet, en raison de la courte longueur uréthrale, les femmes ont un risque accru d’envahissement tumoral de l’urèthre. D’autre part, elles sont à haut risque d’incontinence urinaire sévère après entéroplastie. Cependant, cette notion est controversée, et certaines équipes réalisent des entéroplasties de substitution à des patientes très sélectionnées [9].
L’entéroplastie de substitution
L’entéroplastie est devenue la technique de référence. Elle consiste à prélever un greffon iléal et d’en faire une néovessie en le détubulant. Les uretères sont abouchés à cette néovessie, elle-même anastomosée à l’urèthre. Il existe quatre principaux types d’entéroplasties de substitution, selon la longueur d’iléon prélevé et le sens des plicatures [6] : l’entéroplastie de type Camey II, l’entéroplastie en Z (voir figure), l’entéroplastie de Hautmann, et l’entéroplastie de Studer. Les résultats carcinologiques et fonctionnels de ces différentes techniques sont similaires ; leur choix dépend donc des habitudes propres à chaque équipe.
L’avantage majeur de l’entéroplastie de substitution est qu’elle permet d’éviter une stomie urinaire. Aujourd’hui, plus de 60 % des patients ayant une cystectomie pour cancer de vessie ont une entéroplastie de substitution. Dans notre service, par exemple, le taux d’entéroplasties a significativement augmenté ces 15 dernières années. De 1991 à 1996, 144 patients ont eu une cystectomie, dont 59 (41 %) avec entéroplastie. De 1997 à avril 2004, 240 patients ont eu une cystectomie, dont 172 (71,7 %) avec entéroplastie.
Mortalité et morbidité de l’entéroplastie de substitution
Dans les séries récentes, le taux de mortalité précoce après cystectomie-entéroplastie varie entre 1,6 % et 3 % [3,10-12]. Ce taux a beaucoup baissé en 20 ans, puisqu’au début des années 1980 il était de 12 % dans certaines séries [13]. La mortalité est principalement liée aux complications cardio-vasculaires. Elle est donc corrélée aux co-morbidités des patients. De nos jours, le taux de mortalité après entéroplastie de substitution n’est pas plus élevé qu’après dérivation de Bricker [3,10-12].
La durée moyenne de séjour en soins intensifs est comprise, en fonction des séries, entre 1 et 7 jours [3,10-12]. Elle va jusqu’à 14 jours chez les patients d’un âge supérieur à 75 ans [5]. Dans beaucoup d’équipes, le patient regagne sa chambre d’hospitalisation classique le jour même de l’intervention, après quelques heures de surveillance en salle de réveil.
La durée totale d’hospitalisation varie entre 10 et 13 jours [10].
Deux types de complications sont à distinguer : les complications précoces, qui surviennent le premier mois, et les complications tardives, qui surviennent après 1 mois.
Les complications précoces, qui touchent environ 25 % des opérés, sont essentiellement médicales : troubles cardio-vasculaires, embolie pulmonaire, désorientation temporo-spatiale, infections urinaires et pulmonaires [2]. Ces complications sont favorisées par les co-morbidités et l’âge. Les complications précoces chirurgicales sont plus rares. Elles sont résumées dans le tableau 1. Les fistules urinaires, qui sont les plus fréquentes, surviennent dans moins de 6 % des cas. Elles sont secondaires à un défaut d’étanchéité de l’anastomose uréthro-néovésicale, ou d’une anastomose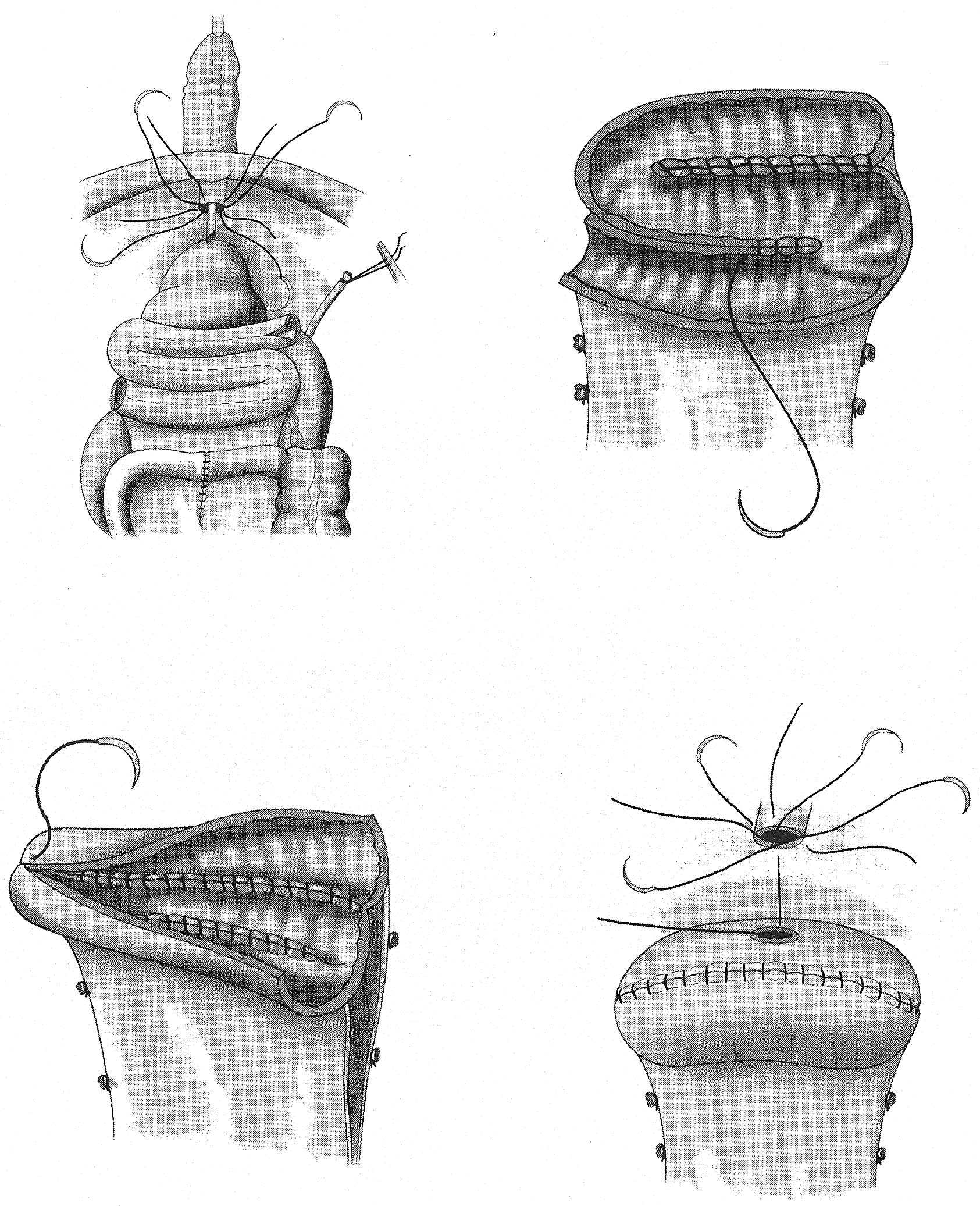
FIGURE — Schémas représentant les étapes de la confection d’une entéroplastie en Z (d’après Zerbib et al . réf. 6).
urétéro-iléale. Le plus souvent, elles peuvent être traitées médicalement, sans réintervention.
Les complications tardives sont essentiellement médicales. Elles sont résumées dans le tableau 2. La complication la plus fréquente est l’apparition de sténoses des anastomoses urétéro-iléales. Celles-ci favorisent la survenue de pyélonéphrites à répétition et d’une insuffisance rénale. Elles sont traitées soit par descente de sondes double J par voie percutanée, soit par réimplantation urétéro-néovésicale.
Résultats carcinologiques de l’entéroplastie de substitution
La cystectomie avec entéroplastie de substitution a les mêmes résultats carcinologiques que la cystectomie suivie d’une dérivation de Bricker. La plus large série la cystectomie a été publiée par l’équipe de Stein en 2001 [3]. Dans cette étude, les résultats de 1054 cystectomies ont été revus avec un recul médian supérieur à 10 ans.
Les taux respectifs de survie sans récidive à 5 et 10 ans étaient, tous stades confondus, de 68 % et 66 %. Chez les patients n’ayant plus de tumeur sur la pièce de cystectomie (résection trans-uréthrale complète), ces taux étaient de 92 % et 86 %.
Chez les patients qui avaient une tumeur T2 résiduelle sur la pièce de cystectomie, sans adénopathie, ces taux étaient de 89 % et 78 %. En revanche, chez les patients qui avaient un envahissement ganglionnaire, ces taux étaient de 35 % et 34 %.
En résumé, la cystectomie permet aujourd’hui un taux de survie sans récidive à 10 ans d’environ 80 %, à condition que le cancer soit limité à la paroi vésicale.
Résultats fonctionnels de l’entéroplastie de substitution
Les séquelles fonctionnelles de la cystectomie avec entéroplastie sont doubles :
sexuelles et urinaires. Chez les hommes, la cysto-prostatectomie radicale supprime les plexus vasculo-nerveux de l’érection, et induit quasi-constamment une impuissance. Il y a deux types de complications urinaires : l’incontinence, et les troubles de la vidange néovésicale.
Les troubles de la vidange néovésicale sont rares. Les facteurs de risque principaux sont la survenue d’une sténose de l’anastomose uréthro-néovésicale (4 % des cas), et l’utilisation d’un greffon iléal de trop grande capacité. Moins de 5 % des patients souffrent de troubles de la vidange vésicale, et moins de 2 % doivent s’auto-sonder [15].
L’incontinence urinaire est plus fréquente. Dans les mois qui suivent l’intervention, elle touche plus de la moitié des patients. Les fuites sont à la fois diurnes et nocturnes. La rééducation vésico-sphinctérienne permet dans la majorité des cas de récupérer une continence compatible avec une activité sociale et professionnelle normale. Les patients se lèvent en général deux fois la nuit pour vider leur néo-vessie, ce qui permet de réduire les fuites nocturnes.
Pour diminuer les séquelles urinaires et sexuelles de la cystectomie chez l’homme, certaines équipes ont modifié la technique en associant à la cystectomie une simple résection trans-uréthrale de prostate. Au lieu de faire l’exérèse complète de la prostate, et de léser ainsi les plexus vasculo-nerveux de l’érection, une simple résection de l’adénome est réalisée. L’entéroplastie n’est donc pas anastomosée à l’urèthre mais à la capsule prostatique. Pour certains, cette technique est recommandée car elle permet d’améliorer le taux de continence et d’érections post-opératoires jusqu’à plus de 80 % [16]. Pour d’autres, cette technique est déconseillée car elle augmente le risque de récidives et de métastases [17].
TABLEAU 1. — Complications chirurgicales précoces de la cystectomie avec entéroplastie, d’après une série de Malavaud et al. incluant 161 patients [14].
Complications
Taux de complications
Taux de réinterventions
Fistule urinaire 5,6 % 2,9 % Éviscération 3,7 % 3,7 % Fistule digestive 2,5 % 2,4 % Iléus prolongé 2,5 % 2,4 % Hémorragie sévère (>5 culots) 1,2 % 0 % TABLEAU 2. — Complications tardives de la cystectomie avec entéroplastie, d’après une série de Zerbib et al. incluant 106 patients [15].
Complications
Taux de complications
Sténoses des anastomoses urétéro-iléales 9,4 % Occlusion du grêle 4 % Sténose de l’anastomose uréthro-néovésicale 4 % Fistule néovésico-cutanée 2,6 % Calculs vésicaux 1,3 % Autosondages 1,3 % Enfin, plusieurs équipes ont évalué la qualité de vie après cystectomie. Les complications urinaires et sexuelles altèrent significativement la qualité de vie, mais les taux de satisfaction rapportés par les patients sont élevés. Par exemple, l’équipe de Bjerre [18] a étudié les résultats fonctionnels et la qualité de vie après cystectomie, en comparant 48 patients ayant eu une entéroplastie de substitution et 29 patients ayant eu une dérivation de Bricker. Seulement 9 % de l’ensemble des patients pouvaient avoir des érections. Après entéroplastie, 18 % des patients avaient des fuites urinaires diurnes, et 21 % avaient des fuites nocturnes. L’indice de satisfaction globale des patients était élevé dans les deux groupes. La qualité de vie sur le plan physique et sexuel était significativement meilleure après entéroplastie.
Conclusions
Aujourd’hui, la cystectomie avec entéroplastie de substitution est le traitement de référence du cancer infiltrant de vessie non métastatique. Grâce aux progrès de l’anesthésie, des techniques chirurgicales, et de la réanimation, l’entéroplastie de substitution a un taux de complications acceptable. En l’absence d’extension extravésicale du cancer, la cystectomie radicale avec entéroplastie de sunstitution s’accompagne d’un taux de survie sans récidive à 10 ans supérieur à 80 %.
BIBLIOGRAPHIE [1] PARKIN D.M., BRAY F.I., DEVESA S.S. — Cancer burden in the year 2000. The global picture.
Eur. J .Cancer. , 2001, 37 , S4-S66.
[2] ZERBIB M., BOUCHOT O., COLOBY P. — Mortalité, morbidité, et résultats fonctionnels de la cystectomie totale. Prog. Urol. , 2002, 12 , 891-911.
[3] STEIN J.P., LIESKOVSKY G., COTE R., GROSHEN S., FENG A.C., BOYD S . et al. — Radical cystectomy in the treatment of invasive bladder cancer : long-term results in 1,054 patients.
J.
Clin. Oncol. , 2001, 19 , 666-675.
[4] ZERBIB M., BOUCHOT O. — Résultats de la cystectomie pour cancer.
Prog. Urol. , 2002, 12 , 913-922.
[5] PEYROMAURE M., GUERIN F., DEBRE B., ZERBIB M. — Surgical management of infiltrating bladder cancer in elderly patients. Eur. Urol. , 2004, 45 , 147-154.
[6] ZERBIB M., SLAMA J., BOUCHOT O.— Dérivation urinaire : techniques chirurgicales.
Prog. Urol. , 2002, 12 , 857-890.
[7] FISCH M., WAMMACK R., MULLER S.C., HOHENFELLNER R. — The Mainz pouch II (sigma rectum pouch). J. Urol. , 1993, 149 , 258-263.
[8] CHANG S.S., COOKSON M.S., BAUMGARTNER R.G., WELLS N., SMITH J.A. JR. — Analysis of early complications after radical cystectomy : results of a collaborative care pathway. J. Urol. , 2002, 167 , 2012-2016.
[9] STENZL A., JAROLIM L., COLOBY P., GOLIA S., BARTSCH G., BABJUK M., et al. — Urethrasparing cystectomy and orthotopic urinary diversion in women with malignant pelvic tumors.
Cancer , 2001, 92 , 1864-1871.
[10] ROSARIO D.J., BECKER M., ANDERSON J.B. — The changing patterns of mortality and morbidity from radical cystectomy. Br. J. Urol. , 2000, 85 , 427-430.
[11] LEBRET T., HERVE J.M., YONNEAU L., BARRE P., LUGAGNE P.M., BUTREAU M., et al. — Étude de la survie après cystectomie pour cancer de la vessie.
Prog. Urol. , 2000, 10 , 533-560.
[12] STUDER U.E., STENZL A., MANSSON W., MILLS R. — Bladder replacement and urinary diversion. Eur. Urol. , 2000, 38 , 790-800.
[13] THOMAS D.M., RIDDLE P.R. — Morbidity and mortality in 100 consecutive radical cystectomies. Br. J. Urol. , 1982, 54 , 716-719.
[14] MALAVAUD B., VAESSEN C., MOUZIN M., RISCHMANN P., SARRAMON J., SCHULMAN C. — Complications for radical cystectomy. Impact of the American Society of Anesthesiologists score. Eur. Urol. , 2001, 39 , 79-84.
[15] ZERBIB M., THIROUARD D., CONQUY S., THIOUNN N., FLAM T., DEBRE B. — Évolution des techniques chirurgicales et résultats des cystectomies à visée curatrice pour cancer de la vessie.
Cancer Radiother , 1998, 2 , 505-511.
[16] VALLANCIEN G., ABOU EL FETTOUH H., CATHELINEAU X, BAUMERT H., FROMONT G., GUILLONNEAU B. — Cystectomy with prostate sparing for bladder cancer in 100 patients : 10-year experience. J. Urol. , 2002, 168 , 2413-2417.
[17] SEBE P., TRAXER O., CUSSENOT O., HAAB F., THIBAULT P., GATTEGNO B. — Cystectomie avec préservation de la prostate dans le traitement des tumeurs vésicales : bases anatomiques, techniques chirurgicales, indications et résultats. Prog. Urol. , 2003, 13 , 1279-1285.
[18] BJERRE B.D., JOHANSEN C., STEVEN K. — Health-related quality of life after cystectomy :
bladder substitution compared with ileal conduit. A questionnaire survey. Br. J. Urol. , 1995, 75 , 200-205.
DISCUSSION
M. Alain LARCAN
Vous n’avez observé heureusement aucun trouble métabolique mais cependant 20 % d’infections urinaires. Ceci me permet d’évoquer les accidents assez spécifiques que l’on observait dans les années 60 après iléocystoplastie ou colocystoplastie avec acidose hyperthermique, coma à répétition et parfois quadriplégie. Nous pensions qu’ils étaient dus à une résorption de chlore sur une surface importante mais toujours associée à une pyélonéphrite ascendante.
Pourriez-vous confirmer l’absence d’infection ascendante du haut appareil ?
Il n’y a pas de pyélonéphrites par reflux car les entéroplasties que nous faisons aujourd’hui sont à basse pression. Les pyélonéphrites que nous voyons aujourd’hui surviennent seulement lorsqu’il existe une sténose de l’anastomose urétéro-iléale (< 10 % des patients).
M. Guy VALLANCIEN
Les complications métaboliques liées à l’isolement de l’anse iléale, ont fait l’objet de nombreuses publications. Tous les urologues connaissent les diarrhées, les deficits en acide folique, les troubles digestifs fonctionnels, et jusqu’à la dramatique acidose métabolique qui peuvent compliquer ces entéro-cystoplasties. Vous semblez indiquer que vous les avez surmontées. Pourriez-vous nous apporter quelques précisions sur ce fait notamment en nous précisant ce que fut votre expérience au fil des années et quelle attitude préventive est aujourd’hui la vôtre pour arriver à cette sécurité ? Quelle expérience avez-vous de la cystectomie avec entéroplastie par voie coelioscopique totale ou assistée ? Pensez-vous qu’il y ait là un moyen de rendre moins lourds, pour le malade, les deux gestes associés de cette chirurgie que sont l’exérèse pour cancer et la reconstruction à visée fonctionnelle ?
Les désordres métaboliques se voyaient il y a 20 ans lorsqu’on réalisait des Bricker de grande taille (30-40 cm). Ces problèmes ont été résolus depuis que nous réalisons des Bricker plus courts (20 cm). De même, les entéro-plasties de substitution ne provoquent plus, aujourd’hui, de troubles métaboliques. Ces troubles se voyaient chez les patients régulièrement infectés (pyélonéphrites par reflux). Le fait qu’il n’y ait plus de reflux néo-vésico-rénal a sûrement réglé également ce problème.
Nous sommes défavorables à la voie laparoscopique pour la cystectomie. Par une incision sous-ombilicale de 8 cm, une cystectomie-entéroplastie dure 2 à 3 heures et le patient sort à J11. Je pense que la laparoscopie ne permettrait pas une durée si courte et des suites si simples. D’autre part, le risque d’essaimage tumoral à l’endroit des trocarts a été largement décrit pour les tumeurs urothéliales.
M. Roger NORDMANN
Parmi les facteurs de risque cités dans la première diapositive, j’ai été surpris de noter l’absence de l’alcool, alors que l’accent a été mis (à juste titre) sur le tabac. Bernard Debré
a cependant, lors d’une réponse, cité la conjonction alcoolo-tabagisme comme facteur essentiel. Ma question se trouve ainsi restreinte à la nature de la boisson alcoolique en cause.
Il a, en effet, été décrit que la consommation de bière serait plus spécifiquement en cause. Les auteurs ont-ils pu avoir des précisions de leurs patients sur ce point particulier ?
Il est vrai que le cancer de vessie survient essentiellement chez les fumeurs, en particulier ceux qui associent l’alcool au tabac. Cependant, à ma connaissance, il n’y a pas plus de risque avec la bière qu’avec les autres alcools.
M. Jean-Daniel SRAER
Le nombre de pyélonéphrites n’est-il pas sous-estimé ? (leur recherche par IRM en montre de latentes) Quelle est la fonction rénale à cinq ans ?
Encore une fois, les seules pyélonéphrites après cystectomie-entéroplastie sont celles qui surviennent en cas de sténose de l’anastomose urétéro-iléale. Il n’y a pas de pyélonéphrites par reflux. Il est vrai qu’environ 20 % des patients vont avoir en post-opératoire une infection urinaire sur sonde. Mais il s’agit d’une bactériurie asymptomatique, et non pas d’une infection du parenchyme rénal.
M. Iradj GANDJBAKHCH
Vous avez communiqué en précisant des pourcentages ? Pouvez-vous nous dire le nombre de patients que vous avez opérés ? Dans quel intervalle et quelles ont été les modifications des résultats au fil des années ?
Le nombre total de cystectomies ainsi que le pourcentage d’entéroplasties augmentent régulièrement. Dans mon service, nous avons fait ces dernières années 60 à 70 cystectomies par an. Le pourcentage d’entéroplasties était de 41 % jusqu’en 1996 ; il est passé à 72 % l’année dernière.
M. Jean NATALI
Quelle est la fréquence des cancers vésicaux de l’homme par rapport à ceux de la femme ?
Lorsque, pour les raisons que vous avez indiquées, vous êtes dans l’obligation d’effectuer une intervention de Bricker, pouvez-vous nous en indiquer brièvement les résultats ?
Le cancer de vessie touche l’homme dans 70 % des cas et la femme dans 30 % des cas. Mais le sexe ratio a tendance à s’équilibrer puisque les femmes fument de plus en plus souvent. Les résultats carcinologiques du Bricker sont les mêmes que ceux de l’entéroplastie, puisque le contrôle carcinologique relève de la cystectomie et non pas du mode de dérivation urinaire. De même, les complications sont similaires : complications médicales en post-opératoire, sténoses de l’anastomose urétéro-iléale et occlusion à distance de l’intervention. En revanche, la qualité de vie est très altérée par le Bricker puisque les patient(e)s doivent s’appareiller.
M. Adolphe STEG
Les auteurs rapportent la fréquence (près de 10 %) des sténoses tardives des anastomoses urétéro-iléales. Celles-ci sont favorisées par la technique qui consiste à recourir à une tunellisation sous muqueuse de l’uretère, dans le but de diminuer le risque de reflux. Ne peut-on pas penser que ce procédé technique est à éviter dans ces néovessies iléales qui sont des réservoirs à basse pression où le risque de reflux, de ce fait, est faible ?
En effet, il n’y a pas d’indication à réaliser un procédé anti-reflux lors de l’implantation des uretères. Cependant, même en faisant une réimplantation directe, il y a un risque de développer une sténose anastomotique d’environ 10 %.
* Service d’Urologie, Hôpital Cochin, 27 rue du faubourg Saint-Jacques, 75014 Paris. Tirés-à-part : Professeur Bernard DEBRÉ, même adresse. Article reçu le 28 juin 2004, accepté le 25 octobre 2004.
Bull. Acad. Natle Méd., 2005, 189, no 1, 123-134, séance du 25 janvier 2005


