Résumé
Pour mieux maîtriser le problème de Santé publique, que représentent les Accidents Vasculaires Cérébraux (AVC), il est important d’évaluer l’évolution de leurs taux d’incidence et de mortalité. Nous avons évalué sur vingt ans, de 1985 à 2004, les variations des taux d’incidence, des taux de mortalité à un mois, de la prévalence des facteurs de risque vasculaires et des traitements préventifs des AVC de novo, à partir de la population non-sélectionnée de la ville de Dijon intra-muros dont 25 % des 150 000 habitants ont plus de 65 ans. Les AVC ont été définis selon leurs deux mécanismes hémorragiques et ischémiques grâce au scanner dans 98 % des cas, complété par l’imagerie en résonance magnétique (IRM) dans 22 % des cas. Nous avons recueilli 3 142 infarctus cérébraux dont 1 708 étaient secondaires à un athérome des grosses artères, 725 secondaires à une lipohyalinose des artérioles perforantes ou infarctus lacunaire, 497 secondaires à une embolie cardioembolique, 212 secondaires à une dissection carotidienne ou vertébrale et 134 d’origine indéterminée, associés à 341 hémorragies cérébrales et 74 hémorragies méningées. En comparant les données par période de cinq ans, on a constaté les résultats suivants : les taux d’incidence standardisés par âge et par sexe des AVC de novo sont restés stables sans variation significative. L’âge moyen de survenue des AVC a significativement reculé de cinq ans chez l’homme, de huit ans chez la femme, confirmant l’augmentation de l’espérance de vie sans AVC. Les taux de mortalité des AVC à vingt-huit jours ont baissé de 10 % chez l’homme âgé de moins de 75 ans (p = 0,01) et ont baissé de 10 % chez la femme âgé de moins de 65 ans (p = 0,03), grâce à la baisse des taux de mortalité des AVC lacunaires (p = 0,05) et hémorragiques (p = 0,03). La répartition des facteurs de risque s’est, elle aussi, profondément modifiée. La prévalence d’hypercholestérolémiques a augmenté de 17 % sur vingt ans (p < 0,01), comme celle des patients diabétiques (p < 0,01). Par contre, la prévalence de patients tabagiques a baissé de 15 % en vingt ans (p < 0,01) comme la prévalence d’antécédents du myocarde qui a baissé de 4 % (p = 0,02). La prévalence d’hypertension artérielle traitée a présenté des variations non significatives (p = 0,62) mais par contre la proportion de patients ayant une HTA diastolique [supérieure à] 90 mmHg baissait de 17 % sur vingt ans (p < 0,01), illustrant le fait que s’ il n’y a pas eu de progrès dans le nombre de patients hypertendus traité, par contre les malades traités ont été mieux contrôlés. Pour la première fois en France, une étude épidémiologique sur une population non-sélectionnée, entreprise sur une très longue période, permet d’évaluer l’évolution des taux d’incidence et de mortalité des AVC. Nous avons observé une chute significative des taux de mortalité à vingt-huit jours chez l’homme et chez la femme, et surtout un recul significatif de l’âge de survenue des AVC de cinq ans chez l’homme et de huit ans chez la femme.
Summary
With progress in stroke prevention it is important to evaluate epidemiological trends over a long period and in an unselected population. We estimated changes in stroke incidence, the case-fatality rate, risk factors, and the use of primary prevention, based on a continuous registry of a well-defined population, from 1985 to 2004. We recorded 3142 ischemic strokes, 341 primary cerebral hemorrhages and 74 subarachnoid hemorrhages. During the 20-year study period, age at first stroke increased by 5 years in men and 8 years in women. Comparing the periods 1985-1989 and 2000-2004, the age — and sex-adjusted incidence rates of first-ever strokes were stable, except for lacunar strokes, the incidence of which increased significantly (p = 0.05), and also cardio-embolic stroke, the incidence of which fell significantly (p = 0.01). Twenty-eight-day case-fatality rates fell significantly, especially for lacunar stroke (p = 0.05) and primary cerebral hemorrhage (p = 0.03).The frequency of hypercholesterolemia and diabetes increased significantly (p < 0.01). In contrast, the frequency of myocardial infarction fell significantly (p = 0.02). The frequency of smoking and diastolic blood pressure J 90 mmHg also fell, but the difference was not significant because of missing data. The frequency of pre-stroke antiplatelet and anticoagulant treatment increased significantly (p < 0.01). The age — and sex-adjusted incidence rates of stroke in Dijon, France, have thus been stable for the past 20 years. Age at stroke onset has increased, the case-fatality rate has fallen, antiplatelet treatment is more frequent, and the frequency of some pre-stroke risk factors has fallen.
INTRODUCTION
Des progrès médicaux réels sont reconnus dans le domaine de la prévention primaire et secondaire des Accidents Vasculaires Cérébraux (AVC) avec la démonstration de l’efficacité du traitement de l’HTA, de l’hypercholestérolémie et le rôle de l’arrêt du tabagisme [1]. Du moins, cette efficacité est démontrée dans des essais thérapeutiques scientifiquement robustes mais ayant pris en compte des populations extrêmement sélectionnées. En est-il de même, en dehors des essais ponctuels, dans la vie quotidienne ?
Cette question mérite d’être posée car les résultats sont contradictoires. Si le déclin des taux de mortalité des accidents ischémiques cardiaques est bien démontré [2], par contre pour les AVC les résultats ne sont pas aussi évidents [3] avec soit une chute soit une élévation du taux de mortalité [4, 5]. Nous observons les mêmes résultats discordants pour les taux d’incidence des AVC [4, 6-10].
A Dijon, nous avons l’opportunité d’avoir un Registre de Population labellisé par l’Inserm et l’Institut de Veille Sanitaire, sur la base de la population de la ville intra-muros qui compte 150 000 habitants et qui enregistre de façon spécifique, exhaustive et continue les AVC quels que soient leur sous-type, l’âge de la population et les modalités de prise en charge en phase aiguë à l’hôpital universitaire, dans l’une des trois cliniques ou à domicile [7].
L’objectif de ce travail est d’analyser l’évolution des taux d’incidence, des taux de mortalité à un mois et de la sévérité des AVC, la distribution des facteurs de risque ayant abouti à l’AVC et des traitements préventifs utilisés avant la survenue de l’AVC, sur une période de vingt ans, de 1985 à 2004.
MATÉRIEL ET MÉTHODES
Nous avons utilisé les mêmes critères diagnostiques et de définition du premier AVC dans la vie du patient et de ses sous-types pendant vingt ans [7].
Population étudiée
Nous avons travaillé sur la base de la population de la ville de Dijon intra-muros de 145 325 habitants en 1985 et 150 138 en 2004. La population des personnes âgées de 75 ans et plus a augmenté de 17 % en vingt ans tandis que la proportion des patients âgés de 85 ans et plus a augmenté de 51 %, illustrant l’augmentation de la population à risque d’AVC.
Recensement des primo-AVC
L’avantage majeur du Registre Dijonnais des AVC est son fonctionnement continu, spécifique et exhaustif sans limitation d’âge et avec la même équipe de recherche depuis vingt ans [7].
La méthodologie, déjà décrite par ailleurs [7], repose sur le recueil de tous les cas au sein de l’Hôpital Universitaire, au sein des trois cliniques de la ville et de la banlieue de Dijon et des cas pris en charge à domicile par les neurologues hospitaliers et libéraux, les médecins généralistes, les cardiologues, les angiologues ou les gériatres.
Les critères de définition des AVC ont été ceux de l’OMS [11] et de la Classification Internationale des Maladies [12]. Les deux mécanismes d’AVC ont été identifiés entre infarctus et hématome cérébral grâce au scanner effectué dans 90 % des cas en
1985 et dans plus de 98 % à partir de 1990, en association avec l’Imagerie en Résonance Magnétique dans 22 % des cas depuis 2000.
Seul un AVC isolé, ou à la rigueur précédé par un Accident Ischémique Transitoire, a été retenu comme de novo et inclus dans le recueil et les calculs [9-13, 14].
L’étude des certificats de décès a permis de recenser les cas décédés prématurément à domicile.
Les facteurs de risque vasculaires précessifs.
Nous avons recueilli les facteurs de risque vasculaires suivants présents avant l’AVC avec les mêmes critères depuis vingt ans (7) :
— l’HTA pour des chiffres J 160/95 mmHg.
— le diabète si la glycémie à jeun était J 7,8 mmol/l ou tout patient traité par insuline ou hypoglycémiants oraux.
— l’hypercholestérolémie pour un taux > 6,0 mmol/l.
— le tabagisme pour les patients fumeurs actuels ou passés, de plus de 1 cigarette/ jour.
— un antécédent d’un AITde moins de 24 h.
— un antécédent d’un infarctus du myocarde ou d’artérite des membres inférieurs, — l’arythmie cardiaque par fibrillation auriculaire diagnostiquée par l’ECG ou par Holter.
— L’échographie transthoracique et transoesophagienne, effectuée pour rechercher une cause d’embolie cardio-cérébrale (valvulopathie, écho spontané, foramen ovale perméable, anévrysme du septum inter-auriculaire, athérome de la crosse aortique) a été réalisée respectivement dans 42,7 % et dans 37,5 %.
— L’écho-Doppler carotidien des artères carotidiennes et vertébrales a été réalisé dans 92,7 % des cas, une angiographie standard dans 5,7 % et en résonance magnétique dans 22,8 % des cas. Un bilan biologique, un bilan de coagulation, un bilan lipidique et un bilan inflammatoire ont été réalisés systématiquement, d’autant qu’ils ont été toujours accessibles tant en secteur hospitalier qu’en secteur libéral.
— Les médicaments consommés avant la survenue d’un AVC furent : les antihypertenseurs, les traitements du diabète, les traitements de l’arythmie cardiaque, l’utilisation d’antiplaquettaires, l’utilisation d’anticoagulants.
Malheureusement, en 1985, les traitements par les hypolipémiants ne furent pas notifiés sur notre fichier.
Diagnostic des types d’AVC.
Les types d’infarctus cérébraux issus des critères TOAST ont été retenus [15, 16] :
— les infarctus cérébraux par athérome des grosses artères cérébrales chez les patients porteurs d’un ou plusieurs facteurs de risque vasculaires, d’un déficit
neurologique de plus de 24 h d’origine cérébrale cortico-sous-corticale, avec une hypodensité visible sur le scanner et touchant le territoire cortico-sous-cortical d’une artère bien définie des hémisphères cérébraux, du tronc cérébral ou du cervelet, le Doppler montrant soit une occlusion, soit une sténose J 70 %, soit des plaques d’athérome authentifiant un athérome avancé des gros troncs arté- riels.
— les infarctus cérébraux d’origine lacunaire par lipohyalinose des petits vaisseaux perforants caractérisés par un syndrome clinique classique comme l’hémiplégie motrice pure proportionnelle, l’hémianesthésie proportionnelle, le syndrome dysarthrie-main malhabile et le syndrome de l’hémiplégie ataxiante avec, sur le scanner ou l’IRM, des infarctus circulaires de moins d’1,5 cm de diamètre situé dans les noyaux gris centraux ou dans la substance blanche.
— les infarctus cérébraux d’origine cardio-embolique chez des patients porteurs soit d’une arythmie cardiaque par fibrillation auriculaire, soit d’un thrombus intracavitaire, d’une valvulopathie ou d’un foramen ovale perméable avec anévrysme du septum inter-auriculaire, soit d’un athérome de la crosse aortique, donnant un déficit neurologique suraigu.
— les infarctus cérébraux par dissection, fréquents avant 60 ans, caractérisés par une cervicalgie, le signe de Claude Bernard Horner, avec sur l’écho-Doppler le flap intimal, sur l’angiographie standard ou en résonance magnétique un rétré- cissement en bec de flûte et sur l’imagerie en résonance magnétique (IRM) en coupes natives l’hématome de la paroi de l’artère.
Les AVC hémorragiques ont été classés en :
— hématomes cérébraux avec l’existence d’un déficit neurologique, brutal avec céphalées ou des vomissements, et sur le scanner une image spontanément hyperdense au sein du parenchyme.
— hémorragie sous-arachnoïdienne avec l’existence d’une céphalée brutale, en casque, accompagnée d’un syndrome méningé avec visualisation du sang dans les espaces sous-arachnoïdiens au scanner ou d’un liquide cérébrospinal sanglant sur 3 tubes.
Quand l’AVC n’avait pas de causes évidentes, une réunion de synthèse était nécessaire pour pouvoir le classer.
Analyse statistique.
— L’évolution des facteurs de risque vasculaires et des médicaments proposés avant l’AVC fut évaluée selon une régression linéaire comparant l’évolution des données sur les 20 ans puis en comparant une à une les quatre périodes de cinq ans (1985-1989, 1990-1994, 1995-1999, 2000-2004) par le test des proportions.
— Nous avons déterminé l’association entre les sous-types d’AVC et chacun des facteurs de risque vasculaires après ajustement à l’âge, au sexe, par une analyse multivariée en régression logistique [9,14].
— Les taux d’incidence bruts et spécifiques par âge et par sexe et les taux standardisés furent calculés par la méthode directe standardisée par rapport à la population française européenne et mondiale [9,14]. Nous avons utilisé la méthode de Poisson pour calculer l’intervalle de confiance à 95 % afin de mesurer les taux d’incidence [9,14]. Une régression exponentielle fut réalisée pour tester l’évolution du temps sur les taux d’incidence d’après ajustement par l’âge et le sexe dans la population de Dijon.
— Les taux de mortalité à 28 jours furent calculés par une régression linéaire. Une analyse univariée par le Test de Student fut effectuée pour les variables continues.
Nous avons complété l’analyse par une régression multivariée pour identifier les variables indépendantes (âge, sexe, sous-type d’AVC, hypertension artérielle, diabète, hypercholestérolémie, antécédent d’AIT, d’infarctus du myocarde et d’artérite des membres inférieurs, arythmie cardiaque par fibrillation auriculaire et la période de temps) qui peuvent influencer les taux de mortalité à 28 jours (variable dépendante). Une valeur de p. < 0.05 fut considérée comme significative.
RÉSULTATS
Distribution des types d’AVC parmi les 3 691 cas recensés.
— Nous avons recensé 1 708 infarctus cérébraux par atteinte des grosses artères (49 %), 725 infarctus cérébraux lacunaires (21 %), 497 infarctus cérébraux d’origine cardio-embolique (14,4 %), 212 infarctus cérébraux par dissection carotido-vertébrale (5,7 %), 134 infarctus cérébraux d’origine indéterminée (3,8 %), 341 hémorragies cérébrales (9,8 %) et 74 hémorragies méningées (2 %).
Le groupe des infarctus cérébraux d’origine indéterminée n’a pas varié au fil des années, en nombre de cas mortels et non mortels.
— Le nombre global d’AVC passa de 875 entre 1985 et 1989 à 972 entre 2000 et 2004 (NS).
— En 1985, l’hôpital universitaire a pris en charge 81,6 % des AVC, les trois cliniques privés 12,2 % et les médecins généralistes 7,1 %, tandis qu’en 2004 les proportions furent 85,7 %, 7,3 % et 6,9 % respectivement.
— L’âge de survenue fut plus élevé chez la femme (71,1 ans chez l’homme versus 75,6 ans chez la femme) reflétant sa plus grande longévité.
— Le fait marquant est le recul significatif de l’âge de survenue des AVC. Il est passé de 66 ans en 1985 à 71,1 ans en 2004 chez l’homme (p = 0,01) et de 67,8 à 75,6 ans (p = 0,01) chez la femme réalisant une espérance de vie sans AVC de cinq ans et plus.
Distribution des facteurs de risque et des traitements précédant la survenue d’un AVC par périodes de cinq ans.
Les facteurs de risque ont présenté une évolution spécifique :
Sont restés stables : (Figure 1) — La prévalence de l’HTA avant l’AVC (p = 0,57) ;
— La tension artérielle systolique moyenne (p = 0,12) ;
— La proportion d’une HTA systolique supérieure à 160 mmHg (p = 0,11) ;
— La proportion des accidents ischémiques transitoires (AIT) (p = 0,12) ;
— La proportion des arythmies cardiaques par fibrillation auriculaire (p = 0,91) ;
— La proportion de l’artérite des membres inférieurs (p = 0,97).
— Il n’y a pas eu de modifications de la prévalence des occlusions des artères cervicales qui est restée stable autour de 6,14 % (fi 3,25 %), de celle des dissections des artères cervicales qui est restée stable aux environs de 5,75 % (fi 2,25 %) et de celle des sténoses des artères carotides > 70 % qui est restée stable aux environs de 7,8 % (fi 3,75 %).
Ont évolué vers la baisse : (Figure 2) — La proportion d’HTA diastolique supérieure à 90 mmHg (p < 0,01) — L’intoxication tabagique (p < 0,01). La proportion des tabagiques chez l’homme était de 63,16 % dans la tranche d’âge 25-35 ans, à 32,58 % au-delà de 75 ans.
Chez la femme, la proportion était de 23,26 % dans la tranche d’âge 25-35 ans, à 4,92 % au-delà de 75 ans.
— la proportion des infarctus du myocarde (p = 0,01).
Ont évolué vers la hausse : (Figure 2) — La prévalence des diabétiques qui augmenta de façon significative (p < 0,01), comme celle de l’hypercholestérolémie (p < 0,01).
Sur le plan des médicaments, la proportion d’HTA traitée par un seul médicament resta stable (p = 0,24), comme celle de l’HTA traitée par deux médicaments (p = 0,51).
Par contre, la proportion d’utilisation d’anti-agrégants augmenta de façon significative (p < 0.01), chez les patients atteints d’un antécédent d’infarctus du myocarde (31 % des cas) ou d’un ou plusieurs facteurs de risque vasculaires (14,4 % des cas), tout comme la proportion d’anticoagulants avant l’AVC (p < 0,01) et exclusivement chez les patients arythmiques. L’augmentation de l’utilisation des anticoagulants est apparue à partir des années 1993-1994, dates des grands essais thérapeutiques préventifs sur l’arythmie cardiaque.
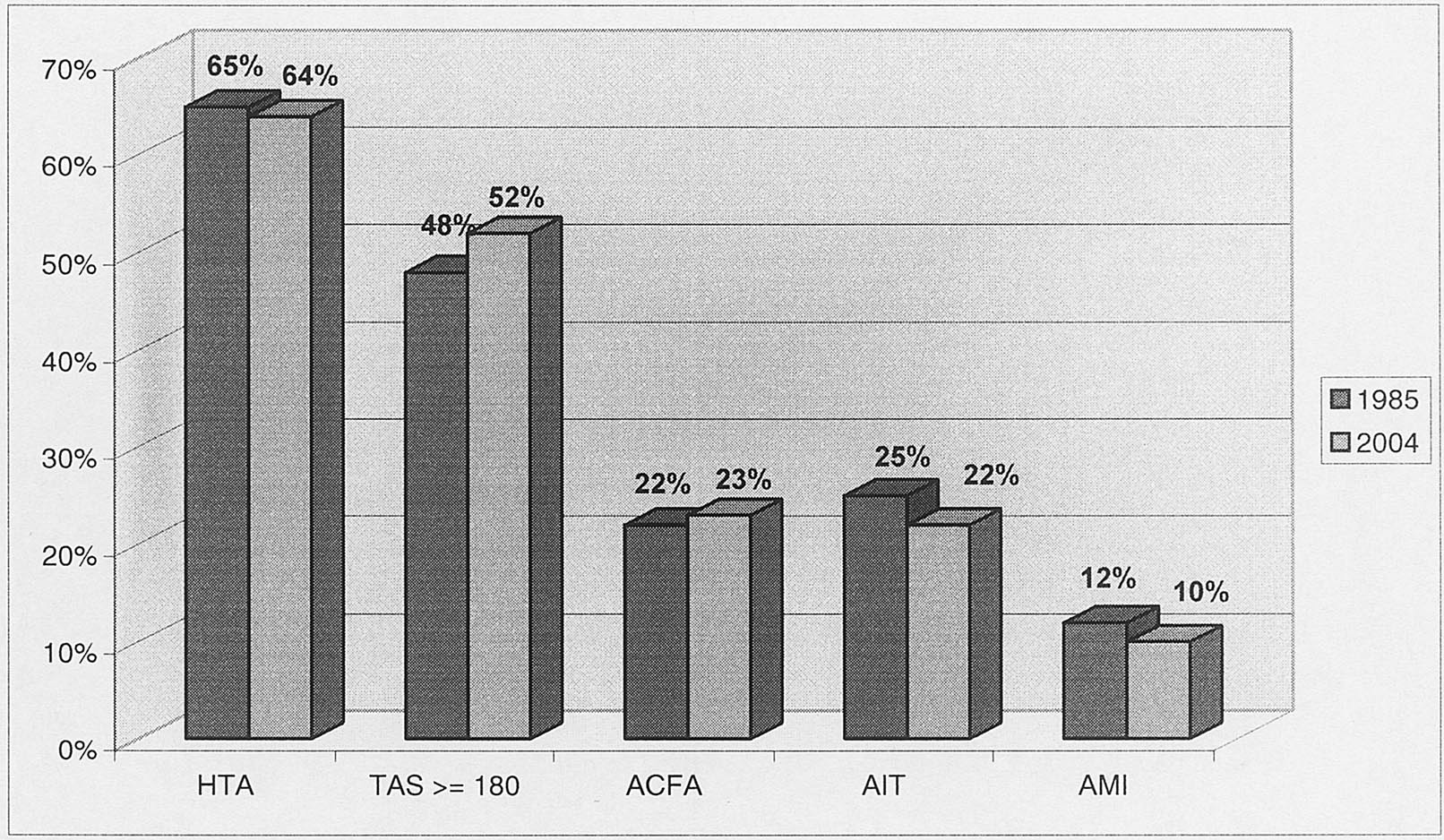
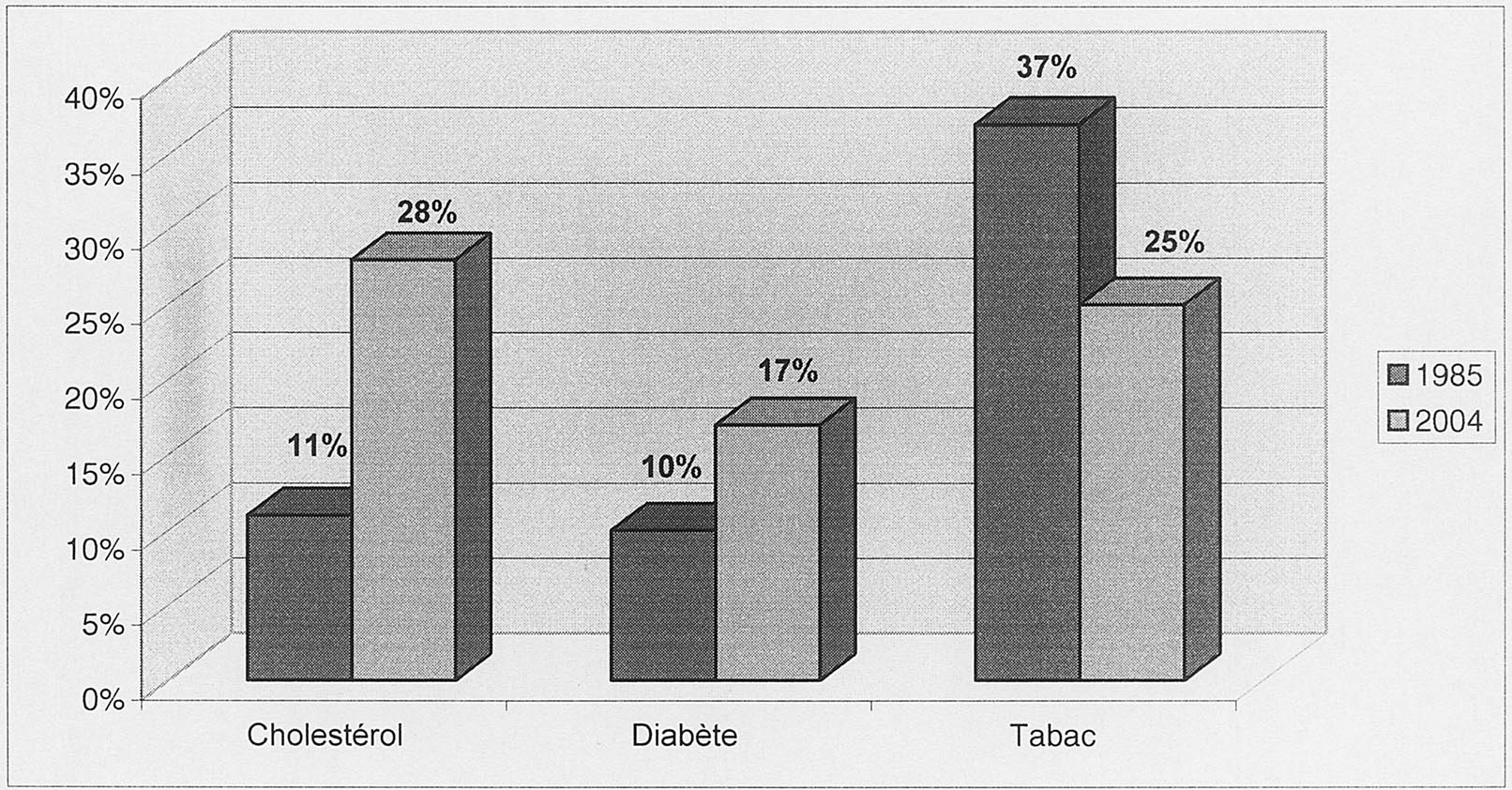
FIG. 1. — Les facteurs de risque qui sont restés stables pendant 20 ans.
FIG. 2. — Les facteurs de risque qui ont évolué.
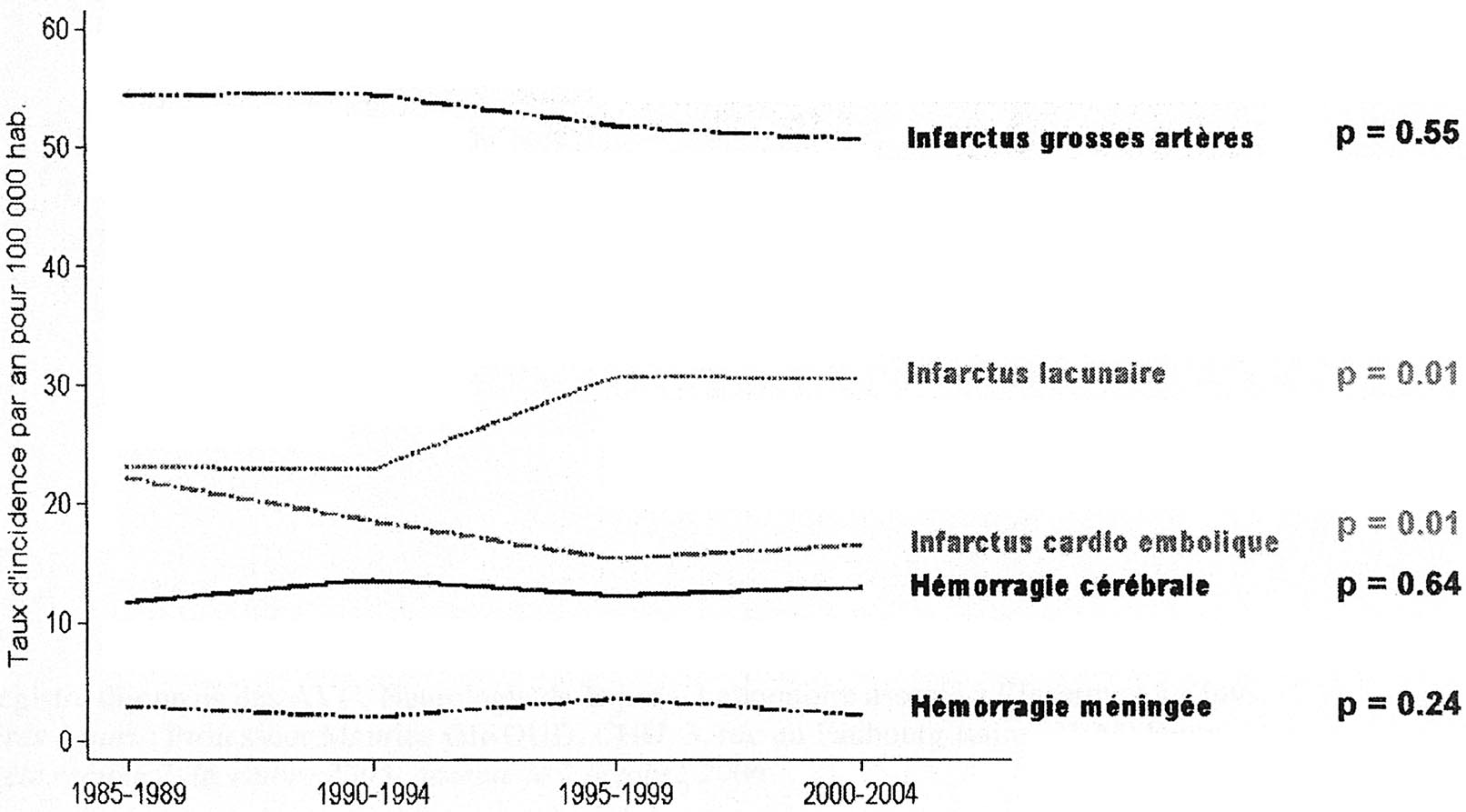
FIG. 3. — Évolution sur 20 ans des taux d’incidence des AVC par sous-type.
Variations des taux d’incidence bruts et standardisés des AVC par période de cinq ans.
— Le tableau 1 rapporte la répartition par nombre absolu, par incidence brute et par période de cinq ans (1985-1989, 1990-1994, 1995-1999, 2000-2004). Le nombre absolu d’AVC a augmenté chez l’homme et chez la femme pendant les vingt années : l’augmentation moyenne était de 2,5 cas par année (CI 95 % = 1,4-3,5, p. < 0,001).
— Les taux d’incidence par âge, par sexe sont rapportés sur les quatre périodes de cinq ans selon la population française (Tableau 2). Les taux d’incidence d’AVC furent plus élevés chez l’homme que chez la femme (p < 0,01) à chaque période sur les vingt années.
— L’évolution des taux d’incidence standardisés durant les vingt années a présenté des fluctuations non significatives chez l’homme et chez la femme. En comparant la première période de cinq années (de 1985 à 1989) à la dernière période de cinq années (de 2000 à 2004) nous n’avons observé aucun changement pour les taux d’incidence chez l’homme (p = 0,46) et chez la femme (p = 0,91). L’évolution des taux d’incidence des AVC de part et d’autre de 85 ans n’a pas changé pendant ces deux périodes. A l’opposé, selon les types d’AVC, si l’élévation de l’incidence des infarctus par athérome des gros troncs artériels n’a pas été significative (p = 0,95), par contre l’incidence des infarctus lacunaires s’est élevée de façon significative de 35 % (p = 0,05) tandis que l’incidence des infarctus cardio-emboliques diminuait de façon significative de 32 % (p = 0,01). Il n’y a pas eu de changement sur l’incidence des hémorragies cérébrales et des hémorragies sousarachnoïdiennes (Figure 3).
.
o v o n e d C V A des CI) % (95 000/an 100 pour brut ’ incidence d taux e t , ge â et e x se par é e é tudi tion popula la de Composition — .
.1 ABLEAU T
.
ç aise an fr tion popula la à pport r a par é s dis standar aux c é r é br es asculair v accidents des bitants ha 000 100 pour uels ann ’ incidence d aux T — 2.
ABLEAU T
TABLEAU 3. — Régression logistique multivariée des facteurs de mortalité à 28 jours.
Évolution des taux de mortalité à 28 jours par période de cinq ans par âge et par sexe.
Les taux de mortalité à vingt huit jours ont chuté de façon très significative pour l’ensemble des AVC sur la période de vingt ans en passant de 17,8 % en 1985 à 10,00 % en 2004 (p < 0,05). Cette chute a été significative chez les hommes de moins de 75 ans avec une décroissance de 13,1 % en 1985 à 3,1 % en 2004 (p = 0,01) et chez la femme de moins de 65 ans avec une décroissance de 13,7 % en 1985 à 3,4 % en 2004 (p = 0,03) (chute de 10 %).
En fonction des types d’AVC, les taux de mortalité à vingt huit jours ont chuté de 4 % pour les infarctus hémorragies cérébrales en passant de 42,6 % en 1985 à 24,5 % en 2004 (p = 0,03) (chute de 24 %). En analyse par régression multivariée (tableau 3), on constate que les types d’AVC, les périodes de cinq ans, la tension artérielle systolique et diastolique, un antécédent d’infarctus du myocarde et l’âge ont un effet significatif sur la chute des taux de mortalité à vingt huit jours. Par contre, le sexe, l’hypercholestérolémie, le diabète, un antécédent d’AIT, l’arythmie cardiaque par fibrillation auriculaire, le tabagisme et l’artérite des membres inférieurs n’ont aucun effet.
Les seuils d’âge différents s’expliquent uniquement par les calculs statistiques.
DISCUSSION
Plusieurs constats seront discutés.
— Le premier constat concerne les changements au niveau de certains facteurs de risque primaires qui ne s’orientent pas tous dans le même sens, nous gardant bien d’en faire une interprétation causale vis à vis des modifications constatées sur les taux d’incidence.
— Pour l’ensemble des AVC, la proportion des patients atteints d’hypercholestérolémie et de diabète a augmenté de façon significative pendant les 20 ans pendant que la proportion des patients atteints de tabagisme, ou présentant une HTA diastolique non contrôlée ou un antécédent d’infarctus du myocarde, a régressé de façon significative. La proportion d’utilisation des anti-angrégants plaquettaires chez les patients athéromateux et des anticoagulants chez les patients arythmiques cardiaques a augmenté, tandis que la proportion d’HTA traitée restait stable.
— L’élévation de la prévalence des patients hypercholestérolémiques et diabétiques est un phénomène observé dans les populations occidentales à cause des régimes alimentaires riches en graisse et en sucre. A l’opposé, la chute du tabagisme est un phénomène bien connu dans les populations âgées comme nous l’avons constaté dans notre travail. La proportion de patients tabagiques, constatée à Dijon, est restée inférieure aux données provenant d’autres études françaises mais concernant des sujets jeunes âgés de moins de 55 ans [17].
— Dans notre étude, nous n’avons pas observé d’augmentation du nombre de patients hypertendus sur les 20 années contrairement à d’autres études (17,18).
La proportion d’un antécédent d’HTA est restée stable entre 1985 et 2004 (61 à 64 %) comme la proportion d’hypertendus traités (48 à 54 %) laissant envisager des progrès en matière de dépistage. La proportion d’HTA systolique> 160 mmHg est restée stable (48 à 52 %) suggérant que si il n’y a pas eu de progrès dans le dépistage de masse de l’HTA à Dijon, par contre les malades hypertendus traités ont été mieux contrôlés.
— Nous avons noté aussi une chute des antécédents d’infarctus du myocarde entre 1985 et 2004. Les données issues de l’étude MONICA ont aussi rapporté un déclin dans l’incidence des infarctus du myocarde pendant la période 1980-1990 [19, 20]. Ce déclin a été attribué à l’amélioration de la prévention avec l’utilisation des inhibiteurs de l’enzyme de conversion, des bêta-bloqueurs et des antiagrégants plaquettaires [20].
— Le progrès le plus sensible est l’augmentation de la proportion de patients arythmiques cardiaques sous anticoagulants sans doute en rapport avec la démonstration dans les années 1990 de l’efficacité de cette thérapeutique en prévention primaire des AVC chez les patients atteints d’une arythmie cardiaque [21].
— Peu d’études sont disponibles pour identifier l’évolution sur une très longue période de la répartition des facteurs de risque cérébro-vasculaires et des médicaments préventifs. L’étude d’Oxford [14] et de Auckland [15] sont les deux études majeures qui ont évalué et observé l’amélioration de la prise en charge des facteurs de risque cérébro-vasculaires (essentiellement l’HTA et le tabagisme) et la meilleure utilisation des médicaments préventifs. Une telle amélioration a été aussi observée mais sur une période plus courte dans des études de population [22], ou hospitalières [23], confirmant le caractère généralisé de l’amélioration des pratiques médicales.
— Le deuxième volet de nos résultats concerne l’évolution des taux d’incidence. Les taux d’incidence bruts sont restés stables tout au long des 2 années de l’étude alors que la population à risque âgée de plus de 85 ans a augmenté significativement, ce qui est en soi un résultat favorable.
— Le constat marquant est le recul significatif de l’âge moyen de survenue des AVC se traduisant par une augmentation de la durée de vie sans AVC de 5 ans chez l’homme et de 8 ans chez la femme, donnée souvent utilisée dans la littérature cancérologique et plus rarement dans la littérature cérébro-vasculaire.
Ce recul de l’âge n’est pas secondaire à l’augmentation de la population à risque car l’incidence des AVC au-delà de 85 ans n’a pas varié. Il s’agit bien d’une augmentation de l’espérance de vie sans AVC.
— L’augmentation des taux d’incidence des infarctus lacunaires pourrait être induite, bien que nous n’ayons pas de preuves, par l’augmentation de la prévalence du diabète et de l’hypercholestérolémie mais aussi à notre capacité d’identifier les petites lacunes avec un meilleur accès à l’IRM cérébrale. Cependant, on rappellera que le taux de couverture scanographique des AVC était déjà très élevé à Dijon, de l’ordre de 90 % dès 1985. Ce phénomène ne peut pas expliquer à lui seul l’augmentation des taux d’incidence des lacunes.
— L’augmentation de l’utilisation des anticoagulants et la chute de l’incidence des infarctus cardio-emboliques semble, par contre, parfaitement liée et en conformité avec les grands essais cliniques des années 1990 [24]. Mais on constate aussi l’élévation du taux d’hémorragies cérébrales associée aux anti-vitamines K.
— Ces changements observés pour les facteurs de risque cérébro-vasculaires et les traitements préventifs sont insuffisants pour expliquer la stabilité des taux d’incidence observés à Dijon. Il y a sans doute d’autres critères pour expliquer nos résultats non retrouvés dans d’autres études [4, 6-8, 25], comme l’alimentation, l’environnement socio-économique, l’accès à la prévention, les comportements et la pollution atmosphérique.
— Enfin, la baisse des taux de mortalité à 28 jours chez l’homme et chez la femme est un progrès médical indiscutable qui relève de nombreux facteurs individuels et collectifs pré-, per- et post-hospitaliers. Les taux de mortalité sont supérieurs chez la femme que chez l’homme comme la plupart des autres études [9, 26, 27].
Les taux de mortalité ont chuté à Dijon chez les hommes âgés et les femmes plus
jeunes, comme cela a été rapporté dans d’autres populations [8,9,14,25], tandis que dans d’autres études plus courtes ce phénomène n’était pas observé [5,28].
Les déterminants de taux de mortalité faibles furent les infarctus lacunaires, la pression artérielle systolique et diastolique basse, l’âge jeune et la survenue des AVC de notre étude entre 2000 et 2004.
— Notre étude présente quelques avantages et quelques limites : notre population était très bien définie sans flux migratoire, sans changement dans la composition ethnique, économique, sociale, sans changement de filière de soins ni d’équipe de recherche. La distribution de types d’AVC est restée tout à fait superposable à celle d’autres pays occidentaux [20, 21].
La cohérence de notre étude de population est la continuité dans les critères diagnostiques, qui sont ceux de l’OMS [7] et qui ont été appliqués de façon stricte, le caractère spécifique et continu de notre recueil reposant sur toutes les filières de pratiques de soins libérales et hospitalières, sur une couverture pratiquement à 100 % par l’imagerie (proche de 90 % dès 1985). Cette cohérence et cette stabilité ont évité des biais de recueil et de diagnostic. A l’opposé, seulement 56 % des AVC recensés à Oxford [14] ont été hospitalisés et il n’est pas évident qu’une imagerie cérébrale ait été effectuée sur chacun des patients. Les mêmes remarques sont aussi valables pour Soderhäm [25] où le diagnostic d’hémorragie cérébrale reposait sur la ponction lombaire entre 1975 et 1977, puis sur le scanner. Il est possible que dans ces 2 études, des cas d’hémorragie cérébrale aient été non diagnostiqués et confondus avec des infarctus cérébraux, problème qui a été évité à Dijon qui essaie de répondre aux critères d’excellence des registres de population pour AVC [29].
— Notre étude s’est déroulée de façon continue, sans arrêt, sur vingt ans alors que l’étude Oxford s’est déroulée [14] de façon discontinue entre 1982 et 1985 et entre 2002 et 2004 avec un long arrêt entre 1985 et 2002. Les mêmes remarques sont applicables à l’étude de Soderhäm [25] qui s’est déroulée de façon discontinue entre 1975 et 1977, 1983 à 1986 et entre 1987 et 1990, et à l’étude de Auckland qui s’est déroulée entre 1980 et 1982, 1991 et 1992 et 2002-2003 [15].
— Nos résultats proviennent d’une population très bien définie sans limite d’âge.
En comparaison, l’étude de Finstroke [9], qui a fait un travail analogue sur quinze ans, a limité sa population en tranche d’âge de 25 et 74 ans, effaçant ainsi les variations induites par les AVC du sujet jeune et du sujet plus âgé.
— À Dijon, nous pensons que le recueil des AVC, et des facteurs de risque cérébro-vasculaires les plus puissants, a été exhaustif (même si nous n’avons pas recensé les syndromes inflammatoires, les syndromes d’apnée du sommeil et les activités physiques). Un doute peut subsister cependant sur l’exhaustivité des AVC pris en charge à domicile mais la forte participation des médecins généralistes et des radiologues réduit ce risque.
— Nos résultats sont ainsi extrêmement intéressants parce qu’ils montrent l’évolution dans le temps de l’incidence des AVC et des facteurs de risque cérébrovasculaires sur une population à risque. Nos résultats, comme ceux d’Oxford [14]
et ceux d’Auckland [15], apportent ainsi le profil spécifique de changements observés sur vingt ans sur l’incidence des AVC et leurs facteurs de risque.
EN CONCLUSION
Ainsi, il s’agit de la première étude de population investiguant l’évolution des taux d’incidence de mortalité sur la base d’un recueil continu sur vingt ans sans restriction d’âge, identifiant tous les types d’AVC grâce à un contrôle en imagerie > 90 %.
Deux faits marquants doivent être soulignés :
— le recul de l’âge de survenue des AVC de cinq ans chez l’homme et de huit ans chez la femme, justifiant l’utilisation du concept de l’augmentation de l’espé- rance de vie sans AVC dans l’évaluation de la prévention primaire des AVC.
— La diminution de la mortalité à Dijon.
BIBLIOGRAPHIE [1] HANKEY G.J., WARLOW C.P. — Treatment and secondary prevention of stroke : evidence, costs, and effects on individuals and populations. Lancet , 1999, 354 , 1457-1463.
[2] WOLF P.A., D’AGOSTINO R.B. — Secular trends in stroke in the Framingham study.
Ann.
Epidemio. , 1993, 3 , 471-475.
[3] FEIGIN V.L., LAWES C.M.M., BENNETT D.A., ANDERSON C.S. — Stroke epidemiology : a review of population-based studies of incidence, prevalence and case-fatality in the late 20th century.
Lancet Neurol. , 2003, 2 , 43-53.
[4] BONITA R., STEWART A., BEAGLEHOLE R. — International trends in stroke mortality : 1970-85.
Stroke , 1990, 21, 989-992.
[5] HARDIE K., JAMROZIK K., HANKEY G.J., BROADHURST R.J., ANDERSON G. — Trends in five-year survival and risk or recurrent stroke after first-ever stroke in the Perth Community Stroke Study.
Cerebrovasc. Dis ., 2005, 19 , 179-185.
[6] STEGMAYR B., ASPLUND K., WESTER P.O. — Trends in incidence, case-fatality rate, and severity of stroke in Northern Sweden, 1985-1991. Stroke , 1994, 25 , 1738-1745.
[7] BENATRU I., ROUAUD O., DURIER J., CONTEGAL F., COUVREUR G., BEJOT Y., OSSEBY G.V., BEN SALEM D., RICOLFI F., MOREAU TH., GIROUD M. — Stable stroke incidence rates but improved case-fatality in Dijon, France, from 1985 to 2004.. Stroke , 2006, 37, 1674-1679.
[8] FEIGIN V.L., WIEBERS D.O., WHISNANT J.P., O’FALLON M. — Stroke incidence and 30-day case fatality rates in Novosibirsk, Russia, 1982 through 1992. Stroke , 1995, 26 , 924-929.
[9] SIVENIUS J., TUOMILHEHTO J., IMMONEN-RÉIHÉ P., KAARISALO M., SARTI C., TORPA J. , et al. —
Continuous 15-year decrease in incidence and mortality of stroke in Finland. The FINSTROKE Study. Stroke , 2004, 35 , 420-425.
[10] MEDIN J., NORDLUND A., EKBERG K. — Increasing stroke incidence in Sweden between 1989 and 2000 among persons aged 30 to 65 years : evidence from the Swedish Hospital Discharge Register. Stroke , 2004, 35 , 1047-1051.
[11] WHO. — The world health report 2000 : Health systems improving performance. Geneva :
WHO , 2000.
[12] National Institute of Neurological Disorders and Stroke Ad Hoc Committee : Classification of Cerebrovascular Diseases III. Stroke, 1990, 21 , 637-676.
[13] BAMFORD J., SANDERCOCK P., DENNIS M., BURN J., WARLOW C. — A prospective study of acute cerebrovascular disease in the community : the Oxforshire Community Stroke Project 1981- 1986, incidence, case fatality and overall outcome at one year of cerebral infarction, primary intracerebral haemorrhage and subarachnoïd haemorrhage. J. Neurol. Neurosurg. Psychiatry , 1990, 53 , 16-22.
[14] ROTHWELL P.M., COULL A.J., GILES M.F., HOWARD S.C., SILVER L.E., BULL L.M. , et al. for the
Oxford Vascular Study. — Change in stroke incidence, mortality, case-fatality, severity and risk factors in Oxfordshire, UK from 1981 to 2004 (Oxford Vascular Study). Lancet , 2004, 363 , 1925-1933.
[15] ANDERSON G.S., CARTER K.N., HACKETT M.L., FEIGIN V., BARBER A., BROAD J.B. , et al , on behalf of the Auckland Regional Community Stroke (ARCOS). – Trends in Stroke incidence in Auckland, New-Zealand, during 1981 to 2003. Study Group, Stroke , 2005, 36 , 2087-2093.
[16] KOLOMINSKY-RABAS P.L., WEBER M., GEFELLER O., NEUDORFER B., HEUSCHMANN P.U. — Epidemiology of ischemic stroke subtypes according to TOAST criteria : incidence, recurrence and long-term survival in ischemic stroke subtypes, a population-based study. Stroke , 2001, 32 , 2735-2740.
[17] ARQUIZAN C., TOUZÉ E., MOULIN T., WOIMANT F., DUCROCQ X., MAS J.L. for the Patent Foramen Ovale and Atrial Septal Aneurysm Study Group. — Blood pressure, smoking and oral contraceptive control after cryptogenic stroke in young adults in the PFO-ASA Study. Cerebrovasc. Dis. , 2005, 20 , 41-45.
[18] JOSEPH LN, BABIKIAN YL, ALLEN NC, WINTER MR. — Risk factor modification in stroke prevention. The experience of a stroke clinic. Stroke ,1999, 30 , 16-20.
[19] TUNSTALL-PEDOE H, KUULASMAA K, MAHONEN M, TOLONEN H, RUOKOKOSKI E, AMOUYEL P.
— Contribution of trends in survival and coronary-event rates to changes in coronary heart disease mortality : 10-year results from 37 WHO MONICA project populations. Monitoring trends and determinants in cardiovascular disease. Lancet , 1999, 353 , 1547-57.
[20] MCGOVERN P.G., JACOBS DR J.R., SHAHAR E., ARNETT D.K., FOLSOM A.R., BLACKBURN H., LUEPKER R.V. — Trends in acute coronary heart disease mortality, morbidity, and medical care from 1985 through 1997 : the Minnesota heart survey. Circulation , 2001, 104 (1) , 19-24.
[21] OSSEBY G.V., BENATRU I., SOCHURKOVA D., URBINELLI R., MEGHERBI S.E., COUVREUR G., MOREAU T., WOLF J.E., GIROUD M. — Trends in utilization of antithrombotic therapy in patients with atrial fibrillation before sstroke onset in community-based study, from 1985 through 1997. From scientific evidence to practice. Preventive Medicine , 2004, 38 ,121-128.
[22] SCHULZ U.G.R., ROTHWELL P.M. — Differences in vascular risk factors between etiological subtypes of ischemic stroke. Importance of population-based studies. Stroke , 2003, 34 , 2050- 2059.
[23] GIROT M., MACKOWIAK-CORDOLIANI M.A., DEPLANQUE D., HÉNON H., LUCAS C. , et al. —
Secondary prevention after ischemic stroke. Evolution overtime in practice.
J. Neurol. , 2005, 252 , 14-20.
[24] DEPLANQUE D., COREA F., ARQUIZAN C., PARNETTI L., MAS J.L ., et al. — SAFE I study investigators. Stroke and atrial fibrillation : is stroke prevention treatment appropriate before hand ? Heart , 1999, 82(5), 563-569.
[25] TERENT A. — Trends in stroke incidence and 10-year survival in Söderham, Sweden, 1975- 2001. Stroke , 2003, 34 , 1353-1358.
[26] THORVALDSEN P., ASPLUND K., KUULASMAA K., RAJAKANGAS A.M., SCHROLL M., for the WHO MONICA Project. — Stroke incidence, case fatality, and mortality in the WHO MONICA project. Stroke , 1995, 26 , 361-367.
[27] AYALA C., CROFT J.B., GREENLUND K.J., KEENAN N.L., DONEHOO R.S., MALARCHER A.M. , et al. — Sex differences in US mortality rates for stroke and stroke subtypes by race/ethnicity and age, 1995-1998.
Stroke , 2002, 33 , 1197-1201.
[28] RYGLEWICZ D., POLAKOWKA M., LECHOWICZ W., BRODA G., ROSZKIEWICZ M. , et al. — Stroke mortality rates in Poland did not decline between 1984 and 1992.
Stroke , 1997, 28 , 752-757.
[29] SUDLOW C., WARLOW C. — Comparable studies of the incidence or stroke and its pathological types : results from an international collaboration. Stroke , 1997, 28 , 491-499.
DISCUSSION
M. Pierre GODEAU
Quelle a été l’évolution post-AVC de cette population concernant le pourcentage de séquelle et l’évolution ou non vers un état de dépendance ou, à l’opposé, la préservation d’une autonomie sans séquelle ? Vous avez fait allusion à l’événement 2Monica2. N’y avait-t-il pas, dans cette étude, une discordance, au profit de Toulouse relativement épargnée, entre la fréquence des accidents coronariens dans le nord et le midi de la France ?
Le taux de dépendance mesuré par le score de Rankin est passé d’une prévalence de 60 % à 49 % ce qui témoigne de la gravité de la maladie malgré les progrès de prise en charge en phase aiguë. Ces progrès sont bien réels comme le confirment les évaluations des unités de soins intensifs neuro-vasculaires qui diminuent la mortalité à un mois de 20 % et qui augmentent le taux de patients totalement autonomes de 20 %. Au sujet des infarctus du myocarde, l’étude Monica-France (Lille, Strasbourg, Toulouse) a montré un gradient nord-sud avec des taux d’incidence et de mortalité des infarctus du myocarde plus élevés dans le nord de la France, ce qui incitera à rechercher la même disparité pour les AVC.
M. Patrice QUENEAU
Parmi les 10 % d’accidents vasculaires cérébraux (AVC) de type hémorragique, quelle est la fréquence des causes iatrogènes induites par l’aspirine, un autre anti-agrégant plaquettaire et/ou une antivitamine K (AVK) ? Parmi les accidents vasculaires cérébraux survenant chez les malades sous AVK, quels sont les pourcentages respectifs des AVC hémorragiques et des AVC ischémiques ? Parmi ces AVC hémorragiques, auriez-vous identifié des accidents induits par l’ajout en automédication d’un anti-agrégant (aspirine notamment) sur un traitement par AVK ?
Les hémorragies cérébrales iatrogènes, induites par les anti-agrégants et les anticoagulants représentent une faible part (5 %) de l’ensemble des hémorragies cérébrales. Sur quatre AVC survenant sous anti-coagulants, 1 seul relève d’une hémorragie cérébrale tandis que trois sur quatre relèvent d’un infarctus cérébral cardio-embolique. Nous n’avons pas de données sur les taux d’hémorragies cérébrales sous l’association anticoagulant — anti-agrégant.
M. Yves CHAPUIS
Ma question rejoint celle de Patrice Queneau quant à la responsabilité des AVC dans les hémorragies. En effet, en 1979, faisant, avec Cl. Mercier, de Marseille, un rapport sur les complications chirurgicales hémorragiques des AVC, nous avions noté un rôle élevé et plausible des AVK dans les hémorragies, lié en partie soit à un mauvais contrôle des AVK, soit dans des indications parfois discutables. Quelle est votre observation dans cette récente expérience ?
Le risque d’hémorragie cérébrale sous AVK reste faible en regard des bénéfices en terme de diminution du risque d’infarctus cérébral chez les patients porteurs d’une arythmie cardiaque par fibrillation auriculaire (diminution du risque de 60 %) ou d’une prothèse valvulaire. Effectivement, pour quatre AVC sous AVK, un seul correspond à une hémorragie cérébrale.
M. Michel ARTHUIS
Avez-vous observé la notion d’AVC sur plusieurs générations ? Je connais une famille avec AVC sur quatre générations.
Effectivement, trois situations sont possibles : — Il peut s’agir d’hémorragies cérébrales sur cavernomatose familiale. — Il peut s’agir d’infarctus cérébraux sur dissection carotido-vertébrale par angio-fibro-dysplasie. — Il peut enfin s’agir d’infarctus céré- braux sous-corticaux avec migraine et déclin cognitif, dans le cadre du syndrome CADASIL (Cerebral Autosomal Dominant Angiopathy with Sub-cortical Infarcts and Leucoencephalopathy).
M. Raymond ARDAILLOU
La relation linéaire entre pression artérielle et fréquence des accidents vasculaires céré- braux comporte-t-elle un seuil ? Y a-t-il une différence entre ce type de relation entre les hémorragies cérébrales et les thromboses vasculaires ?
Il existe un lien linéaire entre l’infarctus cérébral et l’élévation de la TA systolique et diastolique, sans seuil, comme pour le LDL-cholestérol. Par contre, le lien entre TA et hémorragie cérébrale se renforce pour les chiffres élevés de TA systolique et diastolique.
M. Jean NATALI
L’âge moyen de la population est-il resté strictement le même pendant ces vingt-deux ans ?
Sinon, comme cela est probable, quelles ont été vos constatations ?
L’âge moyen de survenu des AVC a reculé de cinq ans chez l’homme et de huit ans chez la femme à Dijon sur la période de vingt-deux ans, traduisant le vieillissement de la population mais aussi l’impact de la prévention primaire qui pourrait ne pas diminuer le risque d’AVC mais simplement retarder son apparition.
M. Michel ARSAC
Avez-vous identifié fissuration ou rupture anévrismales ou micro-anévrismales ? Quelles explorations angiographiques avez-vous effectuées ? Avez-vous observé des phlébites céré- brales ?
Les hémorragies méningées par rupture d’anévrysme ont été aussi recensées. Leurs taux d’incidence et de mortalité sont restés stables pendant vingt-deux ans. Une artériographie standard a été effectuée de façon systématique devant toute hémorragie méningée.
Les phlébites cérébrales ne sont pas recensées dans ce registre traitant des AVC d’origine artérielle.
* Registre dijonnais des AVC, Neurologie de Dijon — Laboratoire associé à l’Inserm et à l’Invs. Tirés à part : Professeur Maurice GIROUD, CHU, 3, rue du Faubourg Rains, 21000 Dijon Article reçu le 2 décembre 2005, accepté le 2 octobre 2006
Bull. Acad. Natle Méd., 2007, 191, no 2, 305-324, séance du 13 février 2007


