Résumé
Le taux d’échec du développement embryonnaire est très important dans notre espèce. On sait depuis longtemps que la cause des fausses couches spontanées est majoritairement chromosomique (66 % des fausses couches). Avec le développement des techniques d’assistance médicale à la procréation, il est devenu possible de rechercher la part des anomalies chromosomiques beaucoup plus tôt, sur les embryons préimplantatoires, ce qui a permis de mettre en évidence un fort taux d’anomalies chromosomiques à ces stades (50 % des embryons conçus). Deux mécanismes ont été identifiés comme étant à l’origine des aneuploïdies ovocytaires, la non-disjonction méiotique (NDM) et la séparation prématurée des chromatides sœurs (SPCS). L’étude du premier globule polaire, cellule complémentaire de l’ovocyte à la méiose, peut être réalisée par la technique d’hybridation fluorescente in situ (FISH) avant injection intra-cytoplasmique de spermatozoïde (ICSI). Ceci a été réalisé dans notre équipe dans deux populations distinctes (patientes âgées de plus de 38 ans et patientes en échec d’implantation) et confirme les résultats obtenus sur les ovocytes non fécondés. Ils permettent également d’affirmer que la SPCS est le mécanisme majoritairement impliqué dans les aneuploïdies liées à l’âge maternel chez l’humain.
Summary
In our species, reproduction failure rate is high. Clinical evidence is miscarriage where chromosomal origin was largely involved (66 % of cases). The development of assisted reproduction techniques made possible to analyse unfertilized oocytes and preimplantation embryos. The results have shown a high rate of chromosome abnormalities before implantation (50 %). Two mechanisms were identified which could generate aneuploidy, the meiosis non-disjunction and the premature separation of sister chromatids (PSSC). A FISH analysis of the first polar body, a cell complementary to the oocyte after meiosis, can be performed before intracytoplasmic sperm injection. We studied 2 distinct populations (patients over 38 years old and patients with recurrent implantation failure) and we confirmed that PSSC is the major mechanism linked to advanced maternal age in human.
INTRODUCTION
L’une des caractéristiques de notre espèce est le mauvais rendement de sa reproduction du fait essentiellement des échecs du développement embryonnaire beaucoup plus fréquents que chez les autres mammifères. Depuis plus de trente ans de très nombreuses études ont été réalisées visant à essayer de comprendre cette spécificité de notre espèce, mais c’est depuis l’avènement des techniques de fécondation in-vitro que les mécanismes commencent à être directement approchés. L’objectif de cette revue est d’apprécier des éléments d’explication des causes et des mécanismes des aneuploïdies embryonnaires, abordées en particulier par l’analyse du premier globule polaire, rendue maintenant possible par la fécondation in vitro .
Importance de la mortalité prénatale : une spécificité de notre espèce, principalement due aux aneuploïdies.
C’est H. Leridon, épidémiologiste, qui a pour la première fois montré de façon explicite qu’il existait dans notre espèce une forte mortalité prénatale [1]. En effet il a recensé toutes les grossesses et leurs issues dans une large cohorte de femmes et a ainsi montré que moins de 40 % des grossesses débutées arrivaient à terme, et que les accidents survenaient très majoritairement durant le premier trimestre de la grossesse.
A et J Boué [2] ont ensuite montré, en réalisant le caryotype de fausses couches spontanées, que 60 % des échecs de la reproduction étaient dus à des anomalies chromosomiques. Ils ont ensuite montré que cette fréquence d’anomalies chromosomiques était beaucoup plus importante parmi les « produits » de fausses couches (60 %) que parmi les « produits » d’interruption volontaire de grossesses (10 %) [3].
Cette étude montrait également la présence de trisomies (présence d’un chromosome en trois exemplaires au lieu de deux) impliquant tous les chromosomes à l’exception du chromosome 1. Par contre aucune monosomie (un exemplaire au lieu de deux) n’a été retrouvée à l’exception de celle du chromosome X (syndrome de
Turner). L’explication de ce phénomène était que les monosomies étaient très peu viables et conduisaient à la survenue de fausses couches très précoces (avant deux semaines). Aujourd’hui il est d’ailleurs admis que l’organisme ne peut vivre avec un déséquilibre de plus de 1 % de son génome en cas de monosomie et 3 % en cas de trisomie. Au total, d’après les résultats de A et J Boué, une extrapolation conduit à estimer à un sur deux le nombre d’embryons aneuploïdes.
Origine des aneuploïdies
Une fois reconnu le taux d’anomalies chromosomiques des embryons humains, différentes équipes ont tenté d’en déterminer l’origine. En étudiant les enfants porteurs de trisomie 13, 18 et 21, ainsi que les fœtus porteurs d’autres trisomies, l’origine majoritairement maternelle des aneuploïdies a été démontrée. Selon T. Hassold [4], 93 % des trisomies 18 sont d’origine maternelle, 95 % des trisomies 21 et 100 % des trisomies 16. De plus ces anomalies surviennent plus particulièrement durant la première division méiotique [5, 6], et l’âge maternel est à ce jour le seul facteur étiologique reconnu dans ce domaine.
Depuis l’avènement des techniques de fécondation in-vitro, l’angle de vision de la fécondation s’est considérablement ouvert, puisque non seulement elle est réalisée dans une « éprouvette », mais de plus on suit l’évolution de l’ovocyte et de l’embryon durant les premiers jours. Malgré le transfert d’embryons de bonne qualité, le taux d’implantation reste en moyenne faible avoisinant les 15 à 20 % [7].
De nombreuses études ont été entreprises pour déterminer les meilleurs critères et différents scores de morphologie embryonnaire ont été proposés, mais leur valeur prédictive reste faible [8-12], ce qui s’explique par le fait que les anomalies chromosomiques n’ont pas encore à ce stade initial de traduction morphologique. Comme l’implantation est une étape de sélection des anomalies chromosomiques, le diagnostic sur embryons préimplantatoires s’est rapidement développé tout au moins dans les pays où il est légalement autorisé.
Données obtenues par l’analyse des embryons préimplantatoires
Les techniques de diagnostic génétique sur cellule unique remontent à environ quinze ans, et les premiers diagnostics préimplantatoires ont été effectués dans la foulée [13, 14]. Les premières approches ont été entreprises sur le globule polaire. Les globules polaires sont issus de la méiose féminine, qui est inégale du point de vue cytoplasmique. Ils ne sont en fait constitués que par les chromosomes entourés d’un peu de cytoplasme. Le premier globule polaire est issu de la division réductionnelle ou première division méiotique, le deuxième de la division équationnelle ou deuxième division méiotique. Toutes les réserves en ARN et protéines se retrouvent dans l’ovocyte. Ainsi, à l’inverse de la méiose masculine qui produit à partir d’une cellule germinale quatre spermatozoïdes ou gamètes de forme identique, la méiose féminine ne produit à partir d’une cellule germinale qu’un seul gamète, l’ovocyte, et deux « rebus » de division méiotique, le premier et le deuxième globule polaire
FIGURE 1. — Schéma de la méiose durant l’ovogenèse.
(figure 1). Seul le partage des chromosomes est effectué de façon identique entre l’ovocyte et les globules polaires.
Rapidement, du fait de la plus grande complexité du diagnostic sur globule polaire, cette approche a été délaissée au profit du diagnostic effectué sur embryon ou diagnostic préimplantatoire. Ainsi de très grandes séries ont été publiées et toutes montrent une très forte proportion d’anomalies chromosomiques dans les populations à risque avec des taux avoisinant les 70 % d’anomalies chromosomiques embryonnaires quand le nombre de chromosomes étudiés est important (9) [15]. Il semble même probable que ce test puisse avoir une valeur pronostique pour le succès futur de l’AMP puisque la plupart des embryons anormaux ne s’implantent pas [16].
Données et limites des analyses des ovocytes
Les techniques de fécondation in-vitro permettent d’obtenir la fécondation d’environ 65 % des ovocytes. Les 35 % restant sont donc des « rebus » et ils sont en général détruits. Néanmoins certaines équipes ont utilisé ces gamètes pour réaliser leur caryotype. Récemment une très grande série de caryotypes d’ovocytes non fécondés a été publiée et elle concluait à la présence de nombreuses anomalies chromosomiques [17] dans les ovocytes non fécondés (20 %) quel que soit l’âge de la patiente, mais à peine 50 % des ovocytes avaient un résultat interprétable. L’idéal serait d’avoir les mêmes informations mais sur l’ensemble de la cohorte ovocytaire.
Les apports de l’analyse des globules polaires
Comme nous l’avons déjà précisé plus haut, les analyses des globules polaires ont été les premières à se développer mais elles ont été rapidement freinées du fait de la complexité de la technique. Or l’étude des globules polaires a l’avantage de refléter, en miroir, la composition chromosomique de l’ovocyte. L’avantage majeur de l’étude du premier globule polaire réside par ailleurs dans la possibilité d’étudier la totalité ou une grande partie de la cohorte ovocytaire et non pas uniquement les ovocytes ayant évolué vers un embryon. Nous avons maintenant une expérience de plus de trois ans dans la pratique de cette technique. Elle nous a permis non seulement d’apporter des précisions sur les mécanismes de constitution des aneu-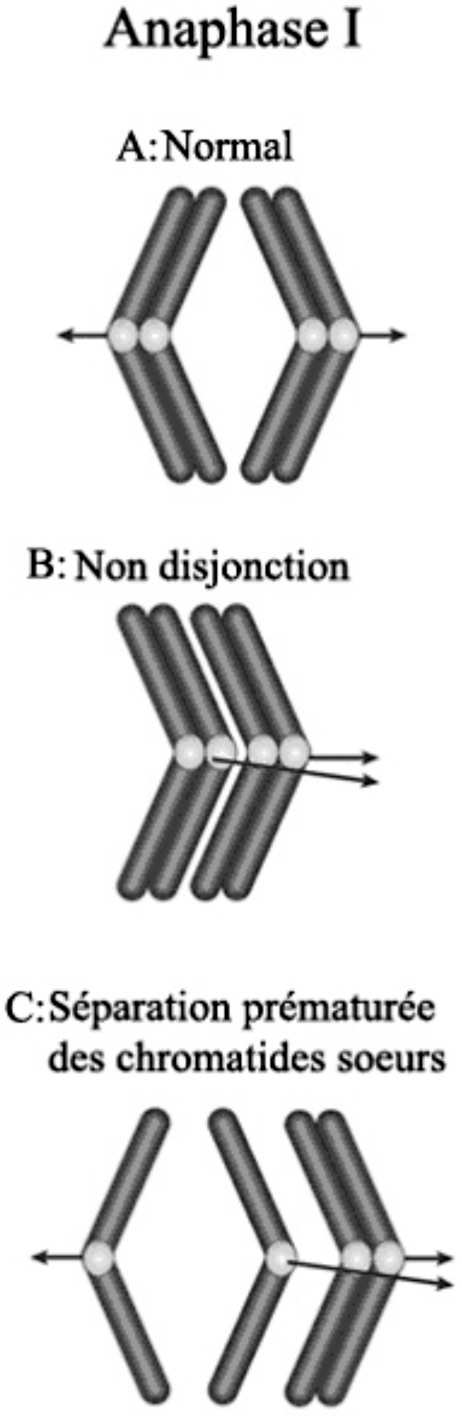
FIGURE 2. — Mécanismes à l’origine des aneuploïdies durant la première division méiotique d’après [6].
Légende A : Cas normal avec migration des deux chromosomes homologues (formés de deux chromatides) vers chaque pôle du fuseau.
B : Non disjonction avec migration des deux chromosomes homologues vers le même pôle du fuseau.
C : Séparation prématurée des chromatides sœurs avec migration de trois chromatides homologues vers un pôle suite à la séparation des deux chromatides d’un des deux chromosomes.
ploïdies, mais de plus de dégager de leurs résultats des indications pronostiques quant aux chances de succès des tentatives ultérieures de FIV.
Les mécanismes de constitution des aneuploïdies
Données de la littérature
Deux mécanismes semblent impliqués dans la survenue de ces anomalies ovocytaires, la non-disjonction méiotique (NDM) et les phénomènes de séparation pré- maturée des chromatides sœurs (SPCS) durant la première division méiotique (figure 2). Un travail récent de Pellestor et al [17] a rapporté une série de 1397 caryotypes d’ovocytes non fécondés après une tentative de fécondation in vitro
(FIV), et montré que le mécanisme le plus fréquemment impliqué dans l’apparition des aneuploïdies était la SPCS (p<0,05). De plus, il semble que la SPCS soit liée de façon plus significative à l’âge de la patiente que la malségrégation [18]. Cette hypothèse avait en fait déjà été émise pour la première fois en 1991 par R. Angell [19].
Néanmoins la population des ovocytes étudiés dans ces séries peut être biaisée puisque les résultats ont été obtenus sur des ovocytes non fécondés après FIV et donc susceptibles plus que les autres d’être porteurs d’une anomalie. De plus une influence de la durée de la culture sur le vieillissement d’un ovocyte in vitro conduisant à des SPCS peut être évoquée [20]. Récemment une étude basée sur l’analyse du premier et du deuxième globule polaire chez des femmes âgées de plus de 35 ans confirmait le rôle prépondérant des SPCS dans la survenue des aneuploïdies fœtales [21]. Mais dans cette étude, encore une fois, la biopsie avait lieu après 20 heures de culture in vitro car elle concernait les deux globules polaires (GP) et un effet de la culture sur le vieillissement du premier globule polaire in vitro ne peut donc être exclu.
Le diagnostic du premier globule polaire avant la mise en fécondation
C’est la technique que nous avons appliquée. A l’inverse des autres études où les analyses ont été effectuées après 48 heures de culture in vitro (ovocytes non fécondés) [17] ou 24 heures (ovocytes fécondés montrant le second globule polaire, et un premier GP « vieilli ») [21] nous avons utilisé des ovocytes frais, immédiatement après recueil, soit une demi-heure à une heure avant la biopsie. Dans ces conditions, il n’existe aucun facteur, autre que l’ovocyte lui-même, permettant d’expliquer une anomalie chromosomique.
Les facteurs de majoration des aneuploïdies • L’âge maternel L’age maternel, est à ce jour, le seul facteur étiologique d’aneuploïdie reconnu. Le risque, évalué en cours de grossesse, augmente fortement à partir de 35 ans (figure 3).
Aussi, pour diagnostiquer plus précocement ces aneuploïdies dès le début du stade embryonnaire, différentes équipes ont proposé de pratiquer chez les femmes âgées de plus de 35 ou 38 ans un Diagnostic Préimplantatoire (DPI). Cette technique devrait, en particulier, permettre de détecter le risque chromosomique chez les patientes âgées ayant recours aux techniques d’assistance médicale à la procréation (AMP). Malgré les résultats favorables des premiers travaux montrant des taux d’anomalies chromosomiques supérieurs à 40 % avec cinq chromosomes analysés [22], une étude randomisée récente [23] montre qu’il n’y a pas de bénéfice, en terme de taux de grossesse, à effectuer un tel examen. On peut voir deux explications à ce résultat décevant, d’une part cette étude avait été faite après la biopsie de deux blastomères, alors qu’un consensus international va maintenant vers la nécessité de ne biopsier qu’un seul blastomère, pour ne pas diminuer les chances de développement de l’embryon, d’autre part comme pour toute étude de FISH, le nombre de chromosome testé était limité aux aneuploïdies viables alors qu’à ce stade les aneuploïdies paraissent toucher tous les chromosomes.
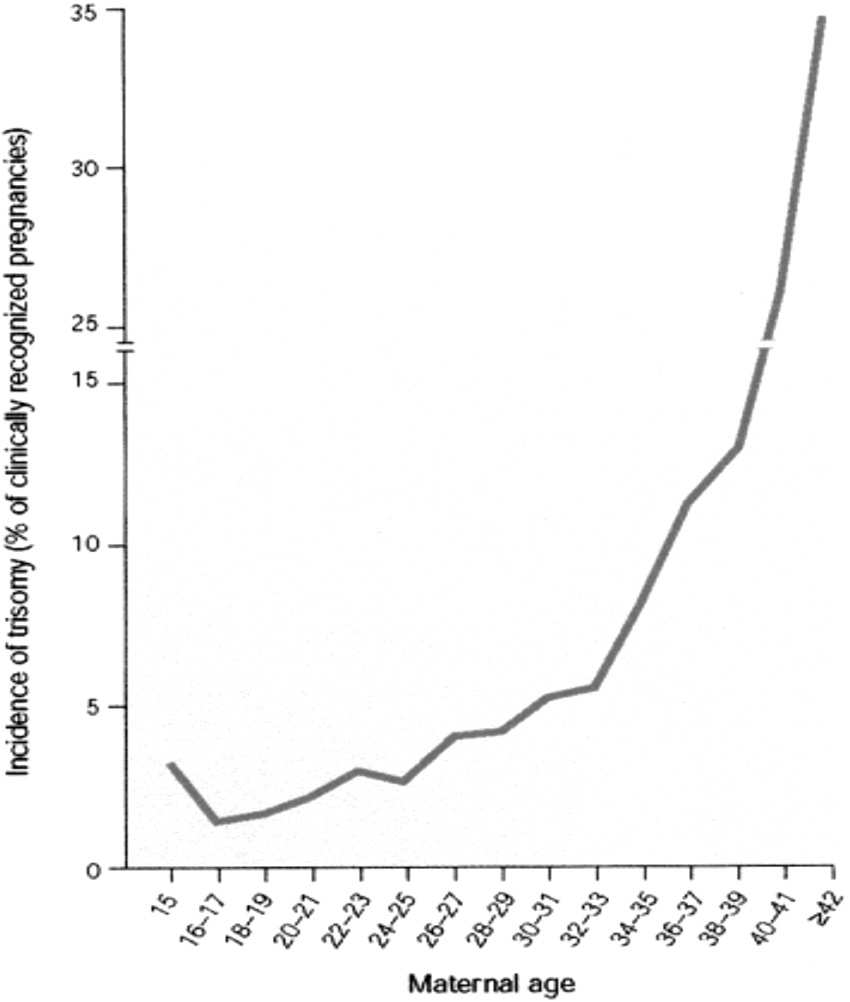
FIGURE 3. — Taux de trisomies en fonction de l’âge maternel.
Légende : Evolution en fonction de l’âge de la mère du pourcentage de trisomies dans les grossesses cliniques [6].
En tous cas, le DPI n’est pas possible en France dans cette situation à risque chromosomique élevé puisque seuls les couples portant une anomalie génétique identifiée ont légalement accès à cette technique. Par contre le diagnostic préconceptionnel (DPC) sur le premier globule polaire, portant sur un gamète et non un embryon, n’est pas interdit. C’est ce que nous avons pratiqué, dans le cadre d’un protocole de recherche, sur des cohortes de complexes « ovocyte-premier globules polaire ». Un des objectifs était d’approcher le mécanisme à l’origine de l’éventuelle aneuploïdie ovocytaire. Dans cette série comportant des patientes ayant un âge moyen de 40 ans (tableau 1) 38,5 % des globules polaires ont été trouvés anormaux et la SPCS représentait 80 % des anomalies. Ce résultat est en accord avec celui de Pellestor [17] qui a identifié 71 % de SPCS sur des ovocytes non fécondés, mais aussi avec l’étude de Kuliev [24] (70 % de SPCS) dans les ovocytes fécondés (femmes de 35 ans ou plus).
• Un autre groupe à risque : les couples en échec d’implantation A coté du groupe des patientes âgées, on peut décrire un autre groupe à risque accru d’anomalies chromosomiques, et sans DPI possible en France, les patientes en échec d’implantation. Il s’agit des patientes n’ayant pas débuté une grossesse clinique
TABLEAU 1. — Résultats de l’analyse du 1er globule polaire dans 2 séries de patientes.
Echec Indication Age maternel d’implantation Nombre de cycles 29 50 Age Moyen 40 ans et 4 mois 35 ans et 11 mois Nombre total de GP analysés 109 221 GP anormal 42 (38,5 %) 96 (43,4 %) Non Disjonction 19/68 (28 %)*
68/143 (47,6 %)*
Anomalies Séparation prématuChromosomiques *
rée des chromatides 49/68 (72 %)*
75/143 (52,4 %)*
sœurs Pourcentage de patientes ayant plus de 1/3 52,5 % 59,5 % des ovocytes anormaux Taux de grossesse par transfert 18,5 % 13 % Légende : L’origine des anomalies chromosomiques est statistiquement différente entre les 2 populations (p<0,01).
malgré le transfert de plus de dix embryons [25]. Ces échecs sont souvent d’origine chromosomique et ces patientes bénéficient maintenant à l’étranger de programme de DPI qui ont confirmé une augmentation du taux d’aneuploïdies embryonnaires [15, 22]. L’interdiction d’une telle pratique en France nous a conduit à proposer à ces couples un diagnostic sur globule polaire. Dans notre série (tableau 1), 43,5 % des globules polaires sont anormaux et 143 anomalies ont été retrouvées. Les deux mécanismes à l’origine des aneuploïdies sont à peux près équivalents en fréquence (43 % de non-disjonction et 57 % de SPCS). Ces résultats sont comparables à ceux de F. Pellestor [17] chez les femmes âgées de moins de 35 ans (47 % de SPCS et 53 % de non-disjonction). Nos résultats confirment donc le rôle important des anomalies chromosomiques dans les échecs d’implantation dans une population de femmes d’âge moyen de 36 ans. Si un taux d’anomalies ovocytaires proche de la population générale (inférieur à 1/3) permet d’écarter une cause chromosomique, un taux compris entre 1/3 et 2/3 et à fortiori un taux supérieur à 2/3 sont en faveur d’une cause chromosomique pour l’échec d’implantation (60 % des patientes dans notre série). Rappelons que nous ne testons sur chaque GP que cinq chromosomes. Si on pouvait tester tous les chromosomes, il est hautement probable que le taux d’ovocytes anormaux serait plus élevé, avec probablement pour certaines patientes une production exclusivement anormale.
Dans ce groupe, à l’inverse du groupe des femmes âgées, les SPCS et les non disjonctions (NDM) sont équivalents en fréquence. Certaines patientes présentent peut être une pathologie de la méiose entraînant des NDM en majorité ou en totalité, situation non retrouvée dans le groupe des patientes âgées de plus de 38 ans.
L’hypothèse d’une altération des mécanismes de ségrégation des quadrivalents, suite à un mauvais appariement, peut être proposée chez ces patientes. Enfin, malgré
un age moyen inférieur de cinq ans, les patientes en échec d’implantation (EI) peuvent présenter une altération globale comparable aux patientes de plus de 38 ans sans EI.
Tentatives d’explication des causes moléculaires des aneuploïdies
Dans la Séparation Prématurée des Chromatides Sœurs (SPCS)
Durant la méiose la cohésion entre les chromatides sœurs implique une classe particulière de protéines, les cohésines [26]. Pendant la transition métaphase / anaphase ces protéines clivent, entraînant le mécanisme de ségrégation chromosomique [27]. Une dégradation prématurée ou un défaut partiel de ces protéines pourrait entraîner une SPCS. De plus une relation entre des petites séquences d’ADN alphoid et des anomalies de la méiose I, et plus particulièrement du chromosome 21 a été démontrée [28, 29]. Cette réduction des séquences pourrait affecter l’association ADN-protéine au niveau des centromères et en particulier les cohésines, altérant ainsi la cohésion des chromatides sœurs. Il a également été montré que le contrôle des « checkpoints » durant la transition métaphase / anaphase était moins efficace chez la femme que chez l’homme [30] et que les ARN messagers des protéines, impliquées dans ce contrôle, subissaient une dégradation en fonction de l’âge [31]. Une altération de la cohésion des chromatides sœurs pourrait donc être due à une réduction des séquences alphoides de l’ADN et/ou une dégradation liée à l’âge des cohésines.
Dans la Non Disjonction Méiotique (NDM)
Les mécanismes sont à l’heure actuelle peu connus. Mais sachant que la disjonction requiert deux protéines essentielles : la Cycline B1 et la securine [32], il est raisonnable de penser que tous les facteurs capables de perturber ces protéines mériteraient d’être étudiés et plus particulièrement dans les cas d’échecs d’implantation.
CONCLUSION
L’analyse du globule polaire a donc un premier intérêt, celui d’apporter des informations sur les mécanismes des aneuploïdies de la première division méiotique qui sont de deux types la non disjonction méiotique et la séparation prématurée des chromatides sœurs. Mais il ne faut pas perdre de vue que ces anomalies ne représentent que 70 % des aneuploïdies d’origine maternelle, et donc que le globule polaire ne donne qu’une vue partielle de la situation. En fait toutes les techniques, que ce soit l’analyse du premier globule polaire, l’analyse du premier et du deuxième globule polaire ou l’analyse des blastomères ont leurs avantages et leurs inconvé- nients. L’analyse du 1er globule polaire a l’inconvénient de n’explorer que la première division méiotique, l’analyse des 2 GP à l’inconvénient de n’être possible qu’après fécondation et d’être réalisée sur un premier globule polaire vieilli avec un
risque de lyse accru. Quant à l’analyse de blastomères, si elle évalue le résultat de l’ensemble de la méiose elle ne le fait que sur les ovocytes fécondés et sans possibilité d’analyser les différents mécanismes.
L’intérêt diagnostique et pronostique de l’analyse du premier globule polaire est également important pour l’évaluation du taux d’aneuploïdies ovocytaire qu’il révèle. Ainsi, dès maintenant, on peut estimer qu’un taux d’anomalies supérieur à 2/3 de l’effectif d’une cohorte a valeur de mauvais pronostic à l’égard d’une tentative ultérieure de FIV. Il est clair qu’une étude d’un plus grand nombre de cas devrait permettre de connaître plus précisément les seuils au-delà desquels il ne serait pas raisonnable de pratiquer des tentatives ultérieures d’aide médicale à la procréation.
Ceci devrait être complété par une étude de la constance du taux d’anomalies ovocytaires d’un cycle à l’autre chez des patientes ayant bénéficié de deux tentatives de ce type. On constate, au total, que outre son intérêt explicatif quant au mécanisme des aneuploïdies, l’analyse du premier globule polaire peut avoir un intérêt pronostique en se substituant au DPI dans des indications encore légalement interdites en France.
BIBLIOGRAPHIE [1] LERIDON H. — Human fertility : the basics components. Univ of Chicago Press, 1977.
[2] BOUE J.G. and BOUE A. — (Frequency of chromosomal aberrations in spontaneous human abortions). Compte Rendu Acad. Sci. Hebd. Seances Acad. Natle. Sci. D. , 1, 1969, 269 (2), 283-8.
[3] BOUE J.G. and BOUE A. — Chromosomal anomalies in early spontaneous abortion. (Their consequences on early embryogenesis and in vitro growth of embryonic cells). Curr. Top. Pathol. , 1976, 62 , 193-208.
[4] HASSOLD T., ABRUZZO M., ADKINS K., et al . — Human aneuploidy : incidence, origin, and etiology.
Environ. Mol. Mutagen. , 1996, 28 (3), 167-75.
[5] PELLESTOR F. — Frequency and distribution of aneuploidy in human female gametes.
Hum.
Genet. , 1991, 86 (3), 283-8.
[6] HASSOLD T. and HUNT P. — To err (meiotically) is human : the genesis of human aneuploidy.
Nat
Rev Genet , 2001. 2(4) : 280-91.
[7] FIVNAT. — Pregnancies and births resulting from in vitro fertilization : French national registry, analysis of data 1986 to 1990. FIVNAT (French In Vitro National).
Fertil Steril ., 1995, 64 , (Oct (4)), 746-56.
[8] EDWARDS R.G., FISHEL S.B., COHEN J., et al . — Factors influencing the success of in vitro fertilization for alleviating human infertility.
J. in. Vitro. Fertil. Embr. Trans. , 1984, 1 , 3-23.
[9] CUMMINS J.M., BREEN T.M., HARRISON K.L., et al . — A formula for scoring human embryo growth rates in in vitro fertilization : its value in predicting pregnancy and in comparison with visual estimates of embryo quality.
J. In. Vitro. Fert. Embryo. Transf. , 1986, 3 (5), 284-95.
[10] PUISSANT F., VAN RYSSELBERGE M., BARLOW P. et al . — Embryo scoring as a prognostic tool in
IVF treatment.
Hum. Reprod ., 1987, 2 (8), 705-8.
[11] SHULMAN A., BEN-NUN I., GHETLER Y., et al . — Relationship between embryo morphology and implantation rate after in vitro fertilization treatment in conception cycles. Fertil. Steril. , 1993, 60 (1), 123-6.
[12] BALAKIER H. and CADESKY K. — The frequency and developmental capability of human embryos containing multinucleated blastomeres. Hum. Reprod. , 1997, 12 (4), 800-4.
[13] VERLINSKY Y., PERGAMENT E. and STROM C. — The preimplantation genetic diagnosis of genetic diseases. J. In. Vitro. Fert. Embryo. Transf. , 1990, 7 (1), 1-5.
[14] STROM C.M., RECHITSKY S. and VERLINSKY Y. — Reliability of gender determination using the polymerase chain reaction (PCR) for single cells. J. In. Vitro. Fert. Embryo. Transf. , 1991, 8 (4), 225-9.
[15] VERLINSKY Y., COHEN J., MUNNE S. et al . — Over a decade of experience with preimplantation genetic diagnosis : a multicenter report.
Fertil. Steril. , 2004, 82 (2), 292-4.
[16] GIANAROLI L., MAGLI M.C., FERRARETTI A.P. et al . — The role of preimplantation diagnosis for aneuploidies.
Reprod. Biomed. Online., 2002 , 4 Suppl 3, 31-6.
[17] PELLESTOR F., ANDREO B., ARNAL F. et al . — Mechanisms of non-disjunction in human female meiosis : the co-existence of two modes of malsegregation evidenced by the karyotyping of 1397 in-vitro unfertilized oocytes. Hum. Reprod. , 2002, 17 (8), 2134-45.
[18] PELLESTOR F., ANDREO B, ARNAL F. et al . — Maternal aging and chromosomal abnormalities :
new data drawn from in vitro unfertilized human oocytes. Hum. Genet. , 2003, 112 (2), 195- 203.
[19] ANGELL R.R. — Predivision in human oocytes at meiosis I : a mechanism for trisomy formation in man. Hum. Genet. , 1991, 86 (4), 383-7.
[20] MUNNE S., DAILEY T., SULTAN K.M. et al . — The use of first polar bodies for preimplantation diagnosis of aneuploidy.
Hum. Reprod. , 1995, 10 (4), 1014-20.
[21] KULIEV A., CIESLAK J., ILKEVITCH Y. et al . — Chromosomal abnormalities in a series of 6,733 human oocytes in preimplantation diagnosis for age-related aneuploidies.
Reprod. Biomed.
Online. , 2003, 6 (1), 54-9.
[22] KAHRAMAN S., BAHCE M., SAMLI H. et al . — Healthy births and ongoing pregnancies obtained by preimplantation genetic diagnosis in patients with advanced maternal age and recurrent implantation failure. Hum. Reprod. , 2000, 15 (9), 2003-7.
[23] STAESSEN C., PLATTEAU P., VAN ASSCHE E. et al . — Comparison of blastocyst transfer with or without preimplantation genetic diagnosis for aneuploidy screening in couples with advanced maternal age : a prospective randomized controlled trial. Hum. Reprod. , 2004, 19 (12), 2849-58.
[24] VERLINSKY Y., CIESLAK J., IVAKHNENKO V. et al . — Prevention of age-related aneuploidies by polar body testing of oocytes.
J. Assist. Reprod. Genet. , 1999, 16 (4), 165-9.
[25] O’NEILL C., FERRIER A.J., VAUGHAN J. et al . — Causes of implantation failure after in-vitro fertilisation and embryo transfer.
Lancet , 1985, 2 (8455), 615.
[26] MICHAELIS C., CIOSK R. and NASMYTH K. — Cohesins : chromosomal proteins that prevent premature separation of sister chromatids. Cell , 1997, 91 (1), 35-45.
[27] WAIZENEGGER I.C., HAUF S., MEINKE A. et al . — Two distinct pathways remove mammalian cohesin from chromosome arms in prophase and from centromeres in anaphase.
Cell , 2000, 103 (3), 399-410.
[28] MARZAIS B., VORSANOVA S.G., ROIZES G. et al . — Analysis of alphoid DNA variation and kinetochore size in human chromosome 21 : evidence against pathological significance of alphoid satellite DNA diminutions. Tsitol. Genet. , 1999, 33 (1), 25-31.
[29] MARATOU K., SIDDIQUE Y., KESSLING A.M. et al . — Variation in alphoid DNA size and trisomy 21 : a possible cause of nondisjunction.
Hum. Genet. , 2000, 106 (5), 525-30.
[30] LEMAIRE-ADKINS R., RADKE K. and HUNT P.A. — Lack of checkpoint control at the metaphase/anaphase transition : a mechanism of meiotic nondisjunction in mammalian females. J. Cell. Biol. , 1997, 139 (7), 1611-9.
[31] STEUERWALD N., COHEN J., HERRERA R.J. et al . — Association between spindle assembly checkpoint expression and maternal age in human oocytes.
Mol. Hum. Reprod. , 2001, 7 (1), 49-55.
[32] HERBERT M., LEVASSEUR M., HOMER H. et al . — Homologue disjunction in mouse oocytes requires proteolysis of securin and cyclin B1.
Nat. Cell. Bio ., 2003, 5 (11), 1023-25.
DISCUSSION
Mme Marie-Odile RÉTHORÉ
Avez-vous étudié l’effet de l’âge de la mère de votre patiente puisque le premier temps de la méïose se passe durant la vie intra-utérine de la femme. Plusieurs publications ont montré que le taux d’aneuploïdies était plus élevé en fonction de l’âge de la mère de la femme alors que l’âge de la mère du père de l’enfant ne joue pas.
Quelques publications ont effectivement montré une augmentation de l’âge de la grandmère maternelle à la naissance des patients atteints de la trisomie 21, alors que la mère était jeune. Nous n’avons, pour notre part, pas étudié ceci. Un travail serait probablement à faire et une telle étude serait réalisable en comparant l’âge des mères de deux groupes, les patientes présentant un taux d’anomalie du premier globule polaire supérieur à 1/3 (taux élevé) et celles avec un taux inférieur à 1/3 (proche de la population générale).
M. Georges DAVID
Certains pays ne sont pas limités, comme la France, pour le recours aux cellules embryonnaires. En pareil cas, les informations obtenues ont-elles des avantages, aussi bien à l’égard de l’explication du mécanisme des aneuploïdies qu’à l’égard de pronostics de tentatives ultérieures ?
Seule l’analyse du premier globule polaire (GP1) est en mesure de nous donner des indications sur le mécanisme à l’origine des aneuploïdies ovocytaires. Dans le cas du dépistage des aneuploïdies sur les blastomères des embryons (PGS), le mécanisme n’est pas abordable. La seule chose que l’on peut rechercher, dans ce cas, est l’origine parentale de l’aneuploïdie (maternelle ou paternelle), et à quelle division méiotique l’anomalie est apparue (méiose I ou II), et ceci par des techniques de biologie moléculaire. En ce qui concerne la valeur pronostique des résultats pour les tentatives de fécondation in vitro ultérieures, une telle étude a déjà été faite pour le PGS, elle concluait au caractère prédictif d’une telle analyse, ceci est tout aussi vrai pour le globule polaire puisque la corrélation entre les résultats de deux tentatives est excellente. L’étude du GP1 a l’avantage de permettre l’analyse de tous les ovocytes des patientes, et non uniquement ceux qui ont été fécondés et ont évolué (soit environ 60 % d’entre eux). Par contre, l’analyse des cellules embryonnaires est plus tardive et permet d’aborder l’ensemble des anomalies provenant de l’ovocyte (après les deux divisions méiotiques) et du spermatozoïde.
* Département de Biologie de la Reproduction, Cytogénétique, Génétique Médicale et Gynécologie Obstétrique, CHI Poissy Saint Germain, 10 rue du Champ Gaillard, 78303 Poissy Cedex. Tirés-à-part : Professeur Jacqueline SELVA, à l’adresse ci-dessus. Article reçu le 22 avril 2005, accepté le 22 juin 2005.
Bull. Acad. Natle Méd., 2005, 189, no 8, 1761-1772, séance du 15 novembre 2005


