Résumé
La section de la moelle épinière est une lésion irréversible. Les axones provenant des cellules mères du cerveau, lors de la repousse après leur section, n’avancent pas vers les motoneurones périphériques. La raison de cette « non-permissivité » au passage de la cicatrice médullaire n’est pas encore claire. Ce travail décrit les tentatives de l’auteur de franchir cet obstacle cicatriciel médullaire grâce à une recherche sur les rats et sur les singes menée par différents protocoles chirurgicaux. Le dernier en date utilise une greffe de nerf sciatique autologue permettant de connecter la substance blanche latérale de la moelle en amont de la lésion directement aux nerfs périphériques propres des muscles paralysés. L’opération a aussi été exécutée sur des êtres humains : volontaires, pleinement informés, atteints d’une section totale de la moelle entre T8 et T11. Le premier cas clinique, opéré par connexion du moignon proximal de la moelle avec les nerfs périphériques, a obtenu une déambulation rudimentaire, fatiguante, mais efficace. La première patiente opérée peut marcher avec des cannes tripodes. La connexion fonctionne, bien que les neurones d’origine des fibres motrices proviennent des régions cérébrales différentes. Ces cellules s’activent simultané- ment et donnent la contraction sélective des différents muscles. Les muscles répondent même si le motoneurone central utilise comme neuro-transmetteur le glutamate (tandis que la plaque motrice normale utilise des récepteurs pour l’acétylcholine). L’analyse par immunoblot de l’ChAT, VAChT, Vglut-1, GluR1 et GluR2 des muscles a montré l’évidence que les récepteurs des plaques motrices passent des Acetilcholinergiques aux Glutamatergiques.
Summary
Spinal cord rupture is still incurable. Axons regenerating from the brain do not advance through the damaged cord towards peripheral motoneurons. The reasons for this ‘‘ nonpermissiveness ’’ are unclear. The author’s research started in 1980 on rats and monkeys, with attempts to connect the lateral tract of the cord, upstream of the lesion, to the muscles, by means of autologous grafts. This operation was subsequently performed on fully informed volunteers with total cord rupture between T8 and T11. The first patient regained a rudimentary but effective gait. This connection of upper motoneurons with peripheral muscle nerves works even when the activating axons derive from cells dispersed among different regions of the brain cortex but that fire together, providing selective contraction of single muscles. Furthermore, this functioning occurs even though upper motor neurons use the neurotransmitter glutamate, whereas motor endplates normally have acetylcholine receptors. In fact, immunoblot analysis of ChAT, VAChT, Vglu-1 GluR1 and GluR2 shows that motor endplate receptors switch from choline to glutamine.
La paraplégie provoquée par une section de la moelle épinière est inguérissable. En effet, la section de la moelle ne permet pas la progression des axones qui régénèrent du cerveau vers les motoneurones périphériques.
Les professeurs dans les écoles de médecine apprennent aux étudiants le dogme que les lésions de la moelle épinière ne peuvent pas guérir. Ce dogme, de toute façon, commence à être contesté par quelques chercheurs qui essayent de surmonter la « non-permissivité » de la moelle épinière.
Les lésions partielles de la moelle épinière peuvent permettre quelque récupération spontanée, mais les lésions complètes, comme celles dues à la luxation vertébrale (avec section en guillotine) sont absolument incurables.
En 1980, je tentais la réparation chirurgicale chez les rats en connectant les deux moignons de la moelle (après résection d’un demi-centimètre) par des greffes de nerfs périphériques autologues. Les greffes étaient ré-habitées par les axones régé- nérants, lesquels toutefois s’arrêtaient dès qu’ils arrivaient de nouveau en contact avec la moelle (système nerveux central : SNC).
Donc après l’axonotomie, les motoneurones centraux régénéraient, mais leur situation au milieu du SNC empêchait leur progression vers leur propre « objectif », c’est-à-dire le bout inférieur.
Les cellules mères restent vivantes et produisent des aminoacides, envoyés à la périphérie vers l’extrémité à reconstruire, c’est-à-dire le squelette des axones détruits par la dégénération Wallerienne, mais elles ne parviennent pas à progresser dans la moelle distale.
Les raisons de cette « non-permissivité » peuvent inclure le manque de cellules de Schwann ou de molécules-guides particulières, l’existence dans le SNC de molécules interdisantes inconnues, la présence d’inhibiteurs, la cicatrice gliale et autres facteurs jusqu’à maintenant inconnus.
La recherche s’effectue dans le monde entier avec pour but de bloquer les inhibiteurs supposés (Nogo Molécules [1]) aussi bien que les molécules de membrane, ou diffusibles, ou de trouver des molécules facilitatrices nouvelles ou de transplanter des cellules supposées favorables : les « olfactory bulb ensheatiang cells), les cellules embryonnaires médullaires, les cellules staminales ou des cellules modifiées génétiquement [2, 3, 4].
Mais, même en admettant que ces cellules puissent former des synapses avec les motoneurones centraux et permettent la repousse des nouveaux axones, il est fort probable que ceux-ci se trouveront eux-mêmes dans un milieu cicatriciel « non permissif » bloquant cette repousse.
D’autres centres cherchent à développer des neuroprothèses sophistiquées avec stimulation électrique des muscles par électrodes implantées activées par ondes électro-encéphalographiques provoquées par des commandes volontaires.
Expérimentation personnelle
Dans mes laboratoires depuis 1981, après avoir vérifié la « non-permissivité » de la moelle en aval de la lésion, j’ai essayé plusieurs protocoles chirurgicaux, négligeant le moignon caudal de la moelle et connectant le moignon rostral avec des nerfs périphériques (dans lesquels les axones sont capables de progresser).
Les axones descendant des faisceaux latéraux (cortico-spinal) seront connectés aux nerfs moteurs de certains muscles sélectionnés grâce à des greffes de nerfs autologues [5, 6, 7]. Nous avons constaté que les motoneurones du SNC progressaient dans les greffes jusqu’aux muscles et formaient de nouveau des plaques motrices en restituant tonus et trophicité. Les muscles répondaient à la stimulation électrique, soit de la greffe, soit de la moelle au-dessus de la lésion.
Ces expériences démontrèrent que le motoneurone supérieur peut produire un axone beaucoup plus long que l’original et reconstruire les plaques motrices. Les expériences sur les rats furent confirmées par des opérations similaires sur trois groupes de singes (macaca fescicularis). Même chez les singes, la recherche a démontré que le motoneurone supérieur peut innerver un muscle séparé de son motoneurone inférieur (Fig. 1).
L’EMG avec stimulation électrique de la greffe et de la moelle démontra de bonnes réponses musculaires avec des temps de latence différents selon la distance entre la stimulation et le muscle (Fig. 2, 3, 4).
La stimulation magnétique du cerveau après craniotomie donna des potentiels évoqués normaux (Fig. 5).
L’histologie des greffes, des nerfs musculaires et des muscles, démontra des aspects semblables à ce que l’on trouve après la réparation des nerfs périphériques (Fig. 6).

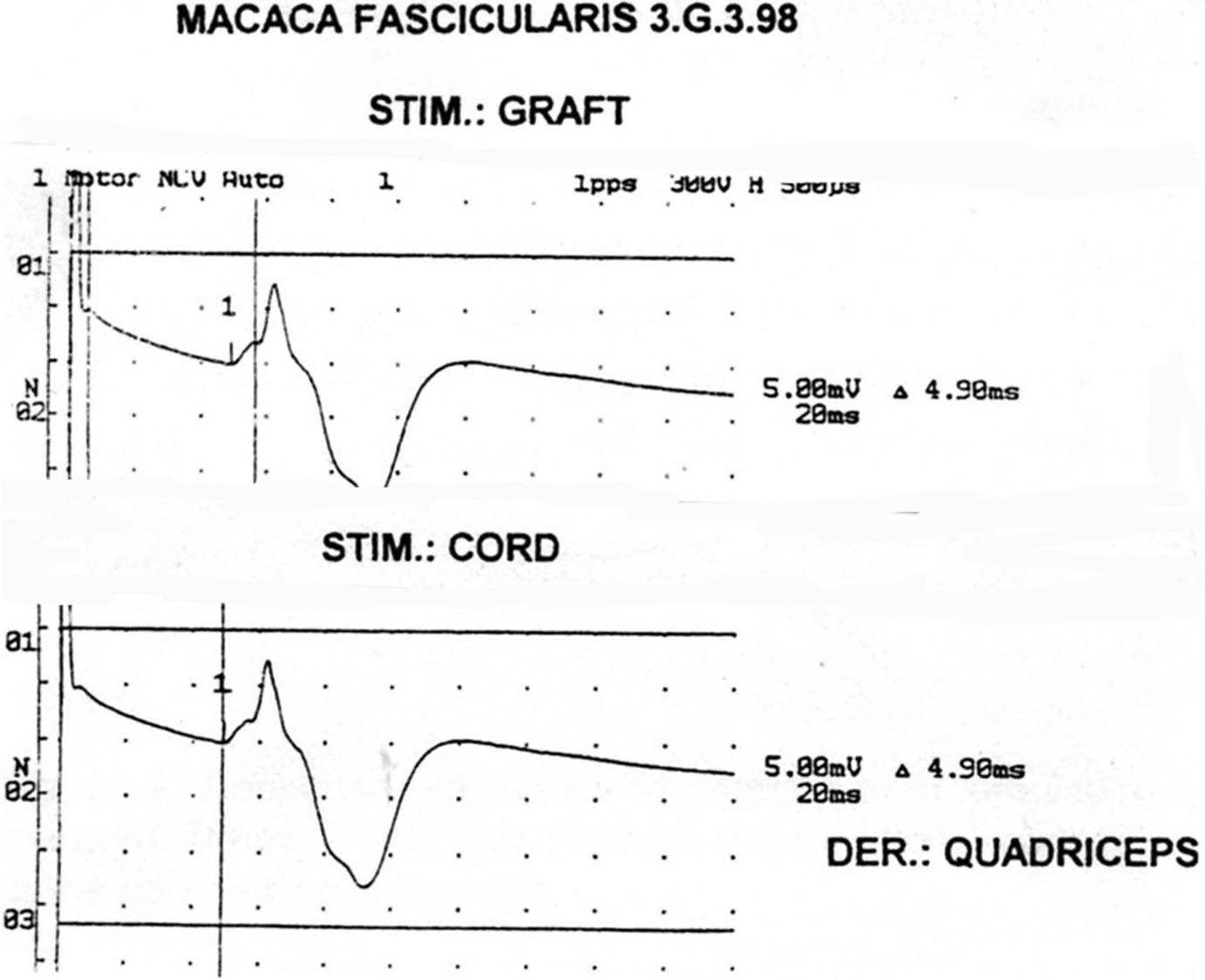
FIG. 1. — Photographie d’un singe après l’opération.
FIG. 2.


FIG. 3.
FIG. 4.
FIGS. 2, 3, 4. — Potentiels d’action dérivés de différents muscles après stimulation de la greffe et de la moelle. Les réponses étaient à peu près identiques. Seule la latence était différente en relation avec la distance entre le point de stimulation et le muscle.


FIG. 5. — Potentiel évoqué d’action motrice après stimulation magnétique du cerveau après craniotomie.
FIG. 6. — Histologie d’une section de la greffe. Aspects similaires à celui d’une greffe dans le SN.
Applications en clinique humaine : premiers cas utilisant le nerf ulnaire
Après l’approbation du Comité d’Ethique du Service Sanitaire National (CESSN) permettant de réaliser une connexion chirurgicale entre SNC et SNP chez l’être humain, nous avons pu chez quatre malades faire le transfert d’un nerf sain du membre supérieur à trois muscles de la hanche (patients tous volontaires avec section totale de la moelle épinière). Le nerf ulnaire a été choisi pour trois raisons (Fig.7, 8) :
— il est assez long pour atteindre les muscles de la hanche.
— il a des branches bien individualisées pour des fonctions différentes, deux branches courtes pour le fléchisseur cubital du poignet et les fléchisseurs profonds de l’auriculaire et deux plus longues pour les muscles hypothénariens, inter-osseux et pour l’adducteur du pouce.
— la paralysie cubitale est facilement corrigée par une chirurgie palliative classique réalisée simultanément avec la chirurgie de la moelle.
Les muscles receveurs étaient le grand fessier, le moyen fessier et le quadriceps. Les critères d’inclusion étaient : la section complète de la moelle (dislocation vertébrale), le niveau de lésion entre T8 et T11 (pour avoir les muscles abdominaux et paravertébraux fonctionnels) et des patients jeunes, maigres, pleins de volonté et de détermination.
Au début les patients, pour obtenir le mouvement des muscles ré-innervés, devaient penser à mobiliser la main, mais bientôt avaient des mouvements de la hanche en pensant à la hanche. Après une longue et contraignante rééducation, le patient présentant le meilleur résultat était capable de se lever de son fauteuil roulant et de marcher 60-70 pas, d’aller à sa voiture et de conduire.
Cas plus récent RELIANT LE SNC AU SNP (nerfs des membres inférieurs paralysés)
J’opérai le premier cas, une jeune femme de 27 ans avec une section totale de la moelle à T8.
La composante péronière du nerf sciatique fut employée bilatéralement pour réaliser un greffon entre la moelle et deux muscles fessiers et le quadriceps.
Après douze mois, les premiers mouvements volontaires étaient présents. À trente six mois, la patiente est capable de se lever toute seule, de marcher pour une courte distance (60-70 mètres) et de repartir après un bref repos. Elle peut marcher avec des cannes quadripodes en ayant abandonné le déambulateur (Fig. 9). Elle peut rester debout plusieurs heures dans sa cuisine.
Par cette opération, les muscles sont complètement détachés des motoneurones inférieurs et connectés seulement avec les motoneurones supérieurs.

FIG. 7. — Schéma du transfert du nerf cubital aux muscles de la hanche.

FIG. 8. — Le patient qui marche avec un déambulateur léger.

FIG. 9. — La patiente opérée par connexion SNC-SNP, qui marche.
— C’est le motoneurone supérieur qui innerve le muscle — La connexion chirurgicale est faite au hasard, de sorte que les axones qui vont à chaque muscle viennent de cellules mères parsemées dans des aires corticales diverses et pourtant elles fonctionnent ensemble, malgré la distance qui les sépare entre elles, et stimulent sélectivement le muscle voulu sans interférences avec les autres muscles.
Études physiopathologiques — Discussion
En conditions normales, le muscle répond au transmetteur du motoneurone infé- rieur utilisant l’Acétylcholine (ACh), alors que par cette opération le muscle répond au motoneurone supérieur lequel normalement utilise un transmetteur différent : le glutamate.
La question à laquelle nous avons cherché à répondre avec une nouvelle expérimentation sur les rats au cours des dernières années était :
le motoneurone supérieur change-t-il de transmetteur ou bien est-ce le muscle qui change de récepteurs ?

FIG. 10. — Schéma de la connexion : en grisé le neurone supérieur, et en clair la greffe qui porte les fibres du neurone supérieur avec les plaques motrices, en pointillé le motoneurone périphérique cholinergique qui est exclu.


FIG. 11. — Potentiels s’action musculaire composés dans le muscle ré-innervé et dans le muscle contrôlé après curarisation.
FIG. 12. — Immunoblot analyse de la ChAt, VAChT et VgluT-1 dans le muscle opéré et dans le muscle contrôle.

FIG. 13. — Présence de récepteurs du glutamate (GluR1 et GluR2) seulement dans le muscle ré-innervé par le neurone supérieur.
Nous avons essayé la stimulation électrique de la greffe après l’administration de vecuronium (bloqueur des récepteurs pour l’Ach) et de GYKI.52466 (antagoniste des récepteurs AMPA pour le glutamate) : les muscles dénervés et connectés avec le motoneurone supérieur étaient bloqués par le GYKI.52466 et non par le vecuronium (Fig. 10), tandis que les muscles contrôles étaient paralysés par le vecuronium.
L’analyse immunoblot de la Cholineacetiltransferase (ChAT), des transporteurs vésiculaires de l’Ach (VAChT) et des transporteurs-1 vésiculaires du glutamate (Vglu-T1) démontra que le muscle dénervé-ré-innervé montrait la présence du Vglu-T1, tandis que le muscle contrôle montrait une positivité par le ChAT et le VAChT et non pour le Vglu-T1. En outre, les récepteurs du glutamate GluR1 et GluR2 étaient présents seulement dans le muscle opéré.
Le traceur injecté dans le muscle opéré se trouvait dans le noyau rouge, démontrant la continuité muscle-greffe-moelle épinière.
En conclusion, il semble que le muscle ré-innervé soit reprogrammé par la transmission glutamatergique pour former des jonctions neuromusculaires glutamatergiques.
CONCLUSION
Ces résultats nous ouvrent des horizons nouveaux et semblent effacer le dogme de l’incurabilité des lésions de la moelle épinière.
Cependant, il faut se méfier de donner des illusions décevantes aux paraplé- giques parce que la solution semble encore très éloignée et difficile et les premiers résultats cliniques sont pauvres, demandent une rééducation très fatigante. Pour le moment, seul un petit nombre de paraplégiques peuvent entrer dans une éventuelle liste d’inclusion.
BIBLIOGRAPHIE [1] CARONI P., SCHAWB ME. — Antibody against myelin associated inhibitor of neurite growth neutralizes non permissive properties of CNS white matter. Neuron, 1988, 1 , 85-96.
[2] AGUAYO AJ., DAVID S., RICHARDSON P., BRAY G. — Axonal elongation in peripheral and central nervous system transplants. Advances in Cellular Neurobiology, 1982, 3 , 215-225.
[3] BJORKLUND A., NORMES H., GAGE FH. et al. — Reinnervation of the denervated spinal cord by grafted noradrenergic and serotenergic brain stem neurons. In Goldberger MF, Gorio A, Murrey M (eds) : Development and Plasticity of the Mammalian Spinal Cord. Padova : Liviana Press , 1986, 291-300.
[4] PANO CL., FERNANDEZ VALLE C., BATES ML., BUBGE MB. — Regrowth of the axons in lesioned adult rat spinal card : promotion by implants of cultured Schwann cells. J. Neurocytol . 199, 23 , 433-452.
[5] BRUNELLI G., MILANESI S. et al. — Innesti per lesioni del midollo spinale. G.I.O.T. , Suppl. 1983, 9 , 53-57.
[6] BRUNELLI G. — Restoration of walking in paraplegia by transfering the ulnar nerve to the hip :
a report on the first patient. Microsurgery, 1999, 19 , 223-226.
[7] BRUNELLI G. — Direct neurotisation of muscles by presynaptic motoneurons.
Jour. Of Reconst.
Microsurgery, 2001, 17 , 8, 631-636.
DISCUSSION
M. Jean CAUCHOIX
Vous réalisez le prodige de réanimer un muscle paralysé : mais ce muscle est spastique. Quel sera son comportement après sa réanimation ?
« Le muscle a perdu sa spasticité après sa séparation du segment distal de la moelle. Il se comporte donc comme tout muscle paralysé.
M. Jacques PHILIPPON
Vous avez montré l’étonnante plasticité des aires corticales primaires. Est-il possible d’utiliser d’autres nerfs périphériques que le nerf cubital (par exemple le nerf intercostal) pour le retour d’une innervation des membres inférieurs ?
« Si l’idée d’utiliser un nerf d’importance fonctionnelle moindre que le nerf cubital tel qu’un nerf intercostal est séduisante sur le plan théorique, elle n’a pas d’intérêt pratiquement car la possibilité d’une commande efficace des mouvements dépend de la relative étendue de la représentation de ce nerf au niveau du cortex primaire : elle est très limitée pour un nerf intercostal.
* Fondazione per la Ricerca Sulle Lesioni del Midollo Spinale, Via Galvani 26, 25126 Brescia — Italie. Tirés-à-part : Professeur Giorgio BRUNELLI, même adresse. Article reçu et accepté le 23 mai 2005.
Bull. Acad. Natle Méd., 2005, 189, no 6, 1135-1149, séance du 7 juin 2005


